
分析 (1)玻璃棒可用于搅拌、引流等作用,根据实验步骤结合玻璃棒的作用来回答;
(2)①草木灰经过柴草燃烧而生成,不可能含有易分解的KHCO3;
②硫酸根离子和盐酸及其钡离子反应生成白色沉淀;
③氯离子和硝酸酸化的银离子反应生成白色沉淀,但是要注意排除CO32-和SO42-的干扰.
解答 解:(1)在溶解固体时,使用玻璃棒可以加速溶解,在过滤操作中,可以用玻璃棒来引流,在蒸发结晶操作中,用玻璃棒来搅拌,使得受热均匀(防止液体飞溅),
故答案为:①②③⑤;
(2)①因为草木灰经过柴草燃烧而生成,不可能含有易分解的KHCO3,所以猜测草木灰中含有钾盐是KHCO3是错误的,故答案为:草木灰经过柴草燃烧而生成,不可能含有易分解的KHCO3;
②向原溶液中先滴加稀盐酸后,再加入BaCl2溶,排除了其它离子的干扰,如果产生白色沉淀,就说明溶液中有硫酸根离子,
故答案为:足量稀盐酸后,再加入BaCl2溶液;
③先加入足量Ba(NO3)2溶液,根据是否出现沉淀来排除CO32-和SO42-的干扰,再向滤液中加入足量稀硝酸酸化的AgNO3溶液,产生白色沉淀,说明溶液中有氯离子,故答案为:向第三支试管中加入足量Ba(NO3)2溶液,过滤后,再向滤液中加入足量稀硝酸酸化的AgNO3溶液,产生白色沉淀,说明溶液中有氯离子.
点评 本题考查离子的检验、分离提纯题、离子反应的应用等问题,题目难度不大,注意基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能全部透过半透膜 | B. | 所得物质一定为悬浊液或乳浊液 | ||
| C. | 所得混合物一定能导电 | D. | 有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
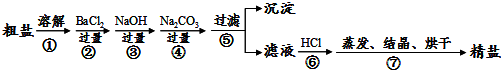
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 | |
| B. | 滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 | |
| C. | 将制得的晶体转移到新制过滤器中用大量水进行洗涤 | |
| D. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
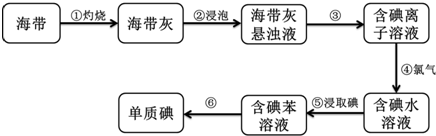
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
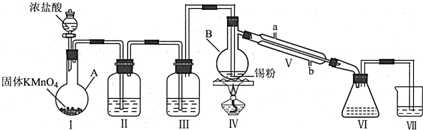
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
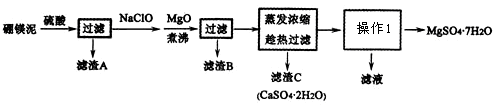
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
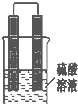 甲同学想利用原电池反应检测金属的活动性顺序,他使用镁片与铝片作电极,放入 稀H2SO4溶液中,如图所示•
甲同学想利用原电池反应检测金属的活动性顺序,他使用镁片与铝片作电极,放入 稀H2SO4溶液中,如图所示•查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com