
某研究小组拟用定量的方法测量Al和Fe分别与酸反应的快慢,设计了如图1所示的装置。

(1)检查图1所示装置气密性的方法是 。
(2)若要比较产生气体的快慢,可以测量相同时间段内产生气体的体积,也可以测量 。
(3)实验测得铝丝产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间段内反应速率逐渐加快的主要原因是 ;t2~t3时间段内反应速率逐渐减慢的主要原因是 。
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:2016-2017学年江西省高二上学期期中化学试卷(解析版) 题型:选择题
下列物质在水溶液中的电离方程式书写正确的是( )
A.CH3COOH===H++CH3COO-
B.NaHSO4===Na++H++SO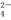
C.H3PO4 3H++PO
3H++PO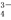
D.NaHCO3 Na++H++CO
Na++H++CO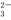
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上期中化学卷(解析版) 题型:选择题
下列叙述中错误的是( )
A.H2SO4的摩尔质量是98
B.等质量的O2和O3中所含氧原子个数相同
C.等物质的量的CO和CO2中所含碳原子数相等
D.2molNO和2mol NO2含原子数不同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上期中化学卷(解析版) 题型:选择题
日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] B.铁制菜刀生锈
C.大理石雕像被酸雨腐蚀毁坏 D.铝锅表面生成致密的薄膜
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上期中化学卷(解析版) 题型:选择题
常温下向纯水中加入少量的硫酸氢钾固体,保持溶液温度不变,则溶液的( )
A.pH值升高 B.碱性减弱
C.水的离子积增大 D.c(OH-)不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上期中化学卷(解析版) 题型:选择题
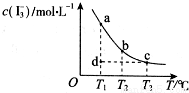
I2在KI溶液中存在下列平衡:I2(aq)+I﹣(aq) I3﹣(aq),某I2、KI混合溶液中,c(I3﹣)与温度T的关系如图所示
I3﹣(aq),某I2、KI混合溶液中,c(I3﹣)与温度T的关系如图所示 (曲线上任何一点都表示平衡状态)。下列说法正确的是( )
(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A.反应 I2(aq)+I﹣(aq) I3﹣(aq)△H>0
I3﹣(aq)△H>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K2>K1
C.若T1时,反应进行到状态d时,一定有υ正>υ逆
D.状态a与状态b相比,状态b时I2的转化率更高
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一上学期期中化学试卷(解析版) 题型:选择题
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含m mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含nmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,则原混合溶液中钾离子的物质的量浓度为( )
A.(4n-2m)/V mol·L-1 B.(n-2m))/V mol·L-1
C.(2n-2m)/ V moI·L-1 D.(n-m)/V mol·L-1
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三12月月考化学试卷(解析版) 题型:实验题
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:

已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl +2H2O。
+2H2O。
(1)若在实验室中煅烧固体混合物,会用到多种硅酸盐质的仪器,除玻璃棒 、酒精灯、泥三角外,还有________(填仪器名称)。流程中多次涉及沉淀,则洗涤沉淀的方法是 。
、酒精灯、泥三角外,还有________(填仪器名称)。流程中多次涉及沉淀,则洗涤沉淀的方法是 。
(2)生产中利用滤渣A制备半导体的反应方程式是_________________。
(3)滤液B中TiOCl 转化生成TiO2的离子方程式是____________________。
转化生成TiO2的离子方程式是____________________。
(4)反应②中固体TiO2转化成(NH4)2Ti5O1 5溶液时,Ti元素的浸出率与反应温度有关,反应温度过高时,Ti元素浸出率会下降,其原因是__________ ____。
5溶液时,Ti元素的浸出率与反应温度有关,反应温度过高时,Ti元素浸出率会下降,其原因是__________ ____。
(5)由滤液D制备LiFePO4的过程中,所需双氧水与H2C2O4的物质的量比是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com