
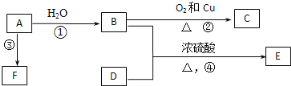
【题目】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)

请回答下列问题:
(1)A的化学式为_____________,丙的化学式为_____________;
(2)写出下列反应的离子方程式:
① _________________________________________;
④ _________________________________________;
⑤ _________________________________________。
(3)写出C溶液与Al反应的化学方程式____________________。
(4)浓硫酸具有强氧化性却可以用B材料车运输,是因为_________________。
(5)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是_____________。
A. 碘水 B. NaOH溶液 C. KSCN溶液 D. Na2SO3溶液
【答案】NaHCl2NaOH+2H2O=2Na++2OH-+H2↑2Fe2++Cl2=2Fe3++2Cl-Fe3++3OH-=Fe(OH)3↓2Al+2NaOH+2H2O=2NaAlO2+3H2↑铁和浓硫酸发生钝化B
【解析】
金属单质A的焰色反应为黄色,则A是Na,黄绿色气体乙是Cl2,Na和水反应生成NaOH和H2,则甲是H2、C是NaOH,氢气和氯气反应生成HCl,所以丙是HCl,D是盐酸,D和金属B反应生成E,E能被氯气氧化生成F,F和NaOH反应生成红褐色沉淀,则红褐色沉淀是Fe(OH)3,所以F是FeCl3、E是FeCl2、B是Fe,再结合物质的性质分析解答。
根据以上分析可知A是Na,B是Fe,C是NaOH,D是盐酸,E是FeCl2、F是FeCl3,甲是H2,乙是Cl2,丙是HCl,红褐色沉淀是Fe(OH)3,则
(1)通过以上分析知,A是Na,丙是HCll;
(2)反应①是Na和水反应生成NaOH和H2,离子反应方程式为2NaOH+2H2O=2Na++2OH-+H2↑;反应④是氯化亚铁和氯气反应生成氯化铁,离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-;反应⑤是氯化铁和氢氧化钠反应生成氢氧化铁,离子方程式为Fe3++3OH-=Fe(OH)3↓;
(3)铝能溶于氢氧化钠溶液生成偏铝酸钠和氢气,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)常温下铁在浓硫酸中钝化,所以浓硫酸虽具有强氧化性却可以用铁质材料车运输;
(5)铁与稀盐酸反应生成氯化亚铁和氢气,则
A. 碘水不能氧化亚铁离子,不能检验亚铁离子,A错误;
B. NaOH溶液与亚铁离子反应生成氢氧化亚铁白色沉淀,然后迅速转化为灰绿色,最终转化为红褐色,可以检验亚铁离子,B正确;
C. KSCN溶液与亚铁离子不反应,不能检验亚铁离子,C错误;
D. Na2SO3溶液与亚铁离子不反应,不能检验亚铁离子,D错误。
答案选B。


科目:高中化学 来源: 题型:
【题目】NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的离子方程式是MnO4-+NO2-+A―→Mn2++NO+H2O(未配平)。下列叙述中正确的是( )
A. 该反应中NO2-被还原
B. 反应过程中溶液的pH减小
C. 反应生成1 mol NO需消耗0.4 mol MnO4-
D. A是OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既能与酸(H+)反应,又能与碱(OH-)反应的化合物是( )
①MgO②Al(OH)3③NaHSO4④NaHCO3⑤CH3COONH4⑥Al
A.②④B.②③④C.②④⑤D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是
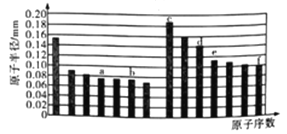
A. a的最高价氧化物与e的最高价氧化物结构相似,都为酸性氧化物且不能与任何酸反应
B. b、c、d、f四种元素的简单离子半径比较: f>b>c>d
C. c、d分别与f组成的化合物均为离子化合物
D. a、f的氧化物对成的水化物酸性及气态氢化物的稳定性f>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F有以下转化关系。A的产量可以衡量一个国家的石油化工发展水平;E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍;F为高分子化合物。结合下图关系回答问题:
(1)写出C的结构简式:___________。
(2)写出B、D中官能团的名称:B____________,D_____________。
(3)写出下列反应的化学方程式:
②_________________________。
④________________________。
(4)物质B可以直接被氧化为D,需加入的试剂是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的无机化工产品之一,在国民经济中占有重要地位。我国采用铁触媒(以铁为主的混合物)做催化剂合成氨。回答下列问题:
(1)Fe基态原子核外电子排布式为____。氮化铁是一种重要的无机化合物,不溶于水,暴露在潮湿环境中可释放出氨气,元素Fe和N中,第一电离能较大的是_____,基态原子核外未成对电子数较多的是_______。
(2)N的氧化物有N2O等,N2O与CO2互为等电子体,N2O的空间构型为__________。
(3)N有多种氢化物,其中肼(N2H4)常用作火箭推进剂的燃料,N2H4中N原子的杂化形式为____。
(4)N、P、As为同族元素,NH3、PH3、AsH3三种物质的沸点由高到低的顺序为_____。原因是____。
(5)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中存在的化学键类型有_______。
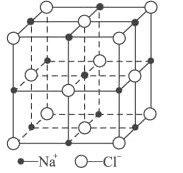
(6)FeO晶体的晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为428pm,则该晶体的密度为____g/cm3(列出计算式即可,用NA表示阿伏加德罗常数的值)。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.若反应X+Y=M是放热反应,该反应一定不用加热
B.CO2与CaO化合是放热反应,则CaCO3分解是吸热反应
C.化学反应伴随的能量有热能和电能二种
D.热值指一定条件下,每1mol的物质完全燃烧所放出的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com