
”¾ĢāÄæ”æ[2017½ĖÕ]ĶعżŅŌĻĀ·“Ó¦æÉ»ńµĆŠĀŠĶÄÜŌ“¶ž¼×ĆŃ(CH3OCH3 )”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
¢ŁC(s) + H2O(g)![]() CO(g) + H2 (g) ¦¤H1 = a kJ”¤mol1
CO(g) + H2 (g) ¦¤H1 = a kJ”¤mol1
¢ŚCO(g) + H2O(g)![]() CO2 (g) + H2 (g) ¦¤H 2 = b kJ”¤mol1
CO2 (g) + H2 (g) ¦¤H 2 = b kJ”¤mol1
¢ŪCO2 (g) + 3H2 (g)![]() CH3OH(g) + H2O(g) ¦¤H 3 = c kJ”¤mol1
CH3OH(g) + H2O(g) ¦¤H 3 = c kJ”¤mol1
¢Ü2CH3OH(g)![]() CH3OCH3 (g) + H2O(g) ¦¤H 4 = d kJ”¤mol1
CH3OCH3 (g) + H2O(g) ¦¤H 4 = d kJ”¤mol1
A£®·“Ó¦¢Ł”¢¢ŚĪŖ·“Ó¦¢ŪĢį¹©ŌĮĻĘų
B£®·“Ó¦¢ŪŅ²ŹĒCO2׏Ō“»ÆĄūÓƵķ½·ØÖ®Ņ»
C£®·“Ó¦CH3OH(g)![]()
![]() CH3OCH3 (g) +
CH3OCH3 (g) +![]() H2O(l)µÄ¦¤H =
H2O(l)µÄ¦¤H =![]() kJ”¤mol1
kJ”¤mol1
D£®·“Ó¦ 2CO(g) + 4H2 (g)![]() CH3OCH3 (g) + H2O(g)µÄ¦¤H = ( 2b + 2c + d ) kJ”¤mol1
CH3OCH3 (g) + H2O(g)µÄ¦¤H = ( 2b + 2c + d ) kJ”¤mol1

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£Ė®ÖŠŌĢ²Ų×Å·įø»µÄ׏Ō“£¬ŌŚŹµŃéŹŅ֊ȔɣĮæŗ£Ė®£¬½ųŠŠČēĻĀĮ÷³ĢµÄŹµŃé£ŗ
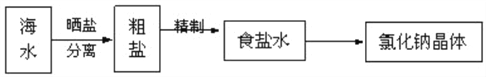
“ÖŃĪÖŠŗ¬Ca2+”¢Mg2+”¢Fe3+”¢SO42©µČŌÓÖŹ£¬Ģį“æµÄ²½ÖčÓŠ£ŗ¢Ł¼ÓČė¹żĮæµÄNa2CO3ČÜŅŗ£»
¢Ś¼ÓČė¹żĮæµÄBaCl2ČÜŅŗ£» ¢Ū¼ÓČė¹żĮæµÄNaOHČÜŅŗ£»¢Ü¼ÓČėŹŹĮæŃĪĖį£» ¢ŻČܽā£» ¢Ž¹żĀĖ£» ¢ßÕō·¢£®ĘäÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ£Ø £©
A. ¢Ż¢Ł¢Ū¢Ś¢Ž¢Ü¢ß B. ¢Ż¢Ł¢Ś¢Ū¢Ž¢Ü¢ß C. ¢Ż¢Ś¢Ł¢Ū¢Ü¢Ž¢ß D. ¢Ż¢Ū¢Ś¢Ł¢Ž¢Ü¢ß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶł·ŠĖ®ÖŠµĪ¼Ó¼øµĪ±„ŗĶFeCl3ČÜŅŗÖŠ£¬ÖʵĆFe(OH)3½ŗĢ壬ŌņĖłµĆ·ÖÉ¢Ļµ(””””)
A. ·ÖÉ¢ÖŹĪŖFeCl3 B. ·ÖÉ¢¼ĮĪŖFe(OH)3
C. ·ÖÉ¢ÖŹĮ£×ÓŠ”ÓŚ1 nm D. ¾ßÓŠ¶”“ļ¶ūŠ§Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³żČ„CO2ÖŠµÄHClŌÓÖŹ×īŗĆŹĒ½«»ģŗĻĘųĢåĶعż×ćĮæµÄ
A£®±„ŗĶNaOHČÜŅŗ B£®±„ŗĶNaHCO3ČÜŅŗ
C£®±„ŗĶNa2CO3ČÜŅŗ D£®Ė®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń.»ÆŗĻĪļMg5Al3(OH)19(H2O)4æÉ×÷»·±£ŠĶ×čČ¼²ÄĮĻ£¬ŹÜČČŹ±°“ČēĻĀ»Æѧ·½³ĢŹ½·Ö½ā£ŗ2Mg5Al3(OH)19(H2O)4![]() 27H2O”ü+10MgO+3Al2O3
27H2Oӟ+10MgO+3Al2O3
£Ø1£©Š“³öøĆ»ÆŗĻĪļ×÷×čČ¼¼ĮµÄĮ½ĢõŅĄ¾Ż____________”£
£Ø2£©ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾³żČ„¹ĢĢå²śĪļÖŠAl2O3µÄŌĄķ________”£
£Ø3£©ŅŃÖŖMgOæÉČÜÓŚNH4ClµÄĖ®ČÜŅŗ£¬ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ĘäŌĄķ_______”£
¢ņ.“ÅŠŌ²ÄĮĻAŹĒÓÉĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ£¬Ä³ŃŠ¾æŠ”×é°“ČēĶ¼Į÷³ĢĢ½¾æĘä×é³É£ŗ

Ēė»Ų“š£ŗ
£Ø1£©AµÄ×é³ÉŌŖĖŲĪŖ_________(ÓĆŌŖĖŲ·ūŗűķŹ¾)£¬»ÆѧŹ½ĪŖ______”£
£Ø2£©ČÜŅŗCæÉČܽāĶʬ£¬Ąż¾ŁøĆ·“Ó¦µÄŅ»øöŹµ¼ŹÓ¦ÓĆ____________”£
£Ø3£©ŅŃÖŖ»ÆŗĻĪļAÄÜÓėĻ”ĮņĖį·“Ó¦£¬Éś³ÉŅ»ÖÖµ»ĘÉ«²»ČÜĪļŗĶŅ»ÖÖĘųĢå(±źæöĻĀµÄĆܶČĪŖ1.518 g”¤L1)£¬øĆĘųĢå·Ö×ӵĵē×ÓŹ½ĪŖ____”£Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½__________”£
£Ø4£©Š“³öF”śG·“Ó¦µÄ»Æѧ·½³ĢŹ½_____________”£Éč¼ĘŹµŃé·½°øĢ½¾æČÜŅŗGÖŠµÄÖ÷ŅŖĪ¢Į£(²»æ¼ĀĒH2O”¢H+”¢K+”¢I)______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲŠĪ³ÉµÄ“æ¾»ĪļA”¢B”¢C”¢D”¢E£¬ĪåÖÖĪļÖŹÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĪļÖŹAÓėĪļÖŹBÖ®¼äµÄ·“Ó¦²»ŌŚČÜŅŗÖŠ½ųŠŠ(EæÉÄÜÓėA”¢BĮ½ÖÖĪļÖŹÖŠµÄŅ»ÖÖĻąĶ¬)”£

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČōCŹĒĄė×Ó»ÆŗĻĪļ£¬DŹĒŅ»ÖÖĒæ¼ī£¬ŌņCµÄ»ÆѧŹ½________£¬²¢ČĪŠ“Ņ»ÖÖCµÄÖ÷ŅŖÓĆĶ¾ ”£
£Ø2£©ČōEµÄĖ®ČÜŅŗ³ŹČõĖįŠŌ£¬DŹĒ¼ČÄÜČÜÓŚĒæĖį”¢ÓÖÄÜČÜÓŚĒæ¼īµÄ»ÆŗĻĪļ”£
¢ŁÓƵēĄė·½³ĢŹ½½āŹĶD¼ČÄÜČÜÓŚĒæĖį”¢ÓÖÄÜČÜÓŚĒæ¼īµÄŌŅņ(½öŠ“³öµēĄė·½³ĢŹ½¼“æÉ)£ŗ ________________________”£
¢ŚÓƵēŗÉŹŲŗćµÄµČŹ½±ķŹ¾EÓėNaOHČÜŅŗ·“Ӧɜ³ÉÕżŃĪµÄČÜŅŗÖŠĖłÓŠĄė×ÓµÄÅضČÖ®¼äµÄ¹ŲĻµ£ŗ________________________________”£
£Ø3£©ČōCŹĒŅ»ÖÖĘųĢ壬DŹĒŅ»ÖÖĒæĖį£¬Ōņ£ŗ
¢ŁCÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________________________”£
¢ŚŅŃÖŖ³£ĪĀĻĀĪļÖŹAÓėĪļÖŹB·“Ӧɜ³É1 molĘųĢåCµÄ¦¤H=£57 kJ”¤mol£1£¬1 molĘųĢåCÓėH2O·“Ӧɜ³É»ÆŗĻĪļDŗĶĘųĢåEµÄ¦¤H=£46 kJ”¤mol£1£¬Š“³öĪļÖŹAÓėĪļÖŹB¼°Ė®·“Ӧɜ³É»ÆŗĻĪļDµÄČČ»Æѧ·½³ĢŹ½ĪŖ__________________________________________”£
¢ŪÓŠČĖČĻĪŖ”°ÅØH2SO4æÉŅŌøÉŌļĘųĢåC”±”£Ä³Ķ¬Ń§ĪŖĮĖŃéÖ¤øĆ¹ŪµćŹĒ·ńÕżČ·£¬ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ锣
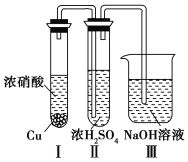
ŹµŃé¹ż³ĢÖŠ£¬ŌŚÅØH2SO4ÖŠĪ“·¢ĻÖÓŠĘųĢåŅŻ³ö£¬ŌņµĆ³öµÄ½įĀŪŹĒ____________________________”£
¢ÜÓĆ²¬×öµē¼«µē½āH2SO4µÄČÜŅŗ£¬ĘäŃō¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÖŠ,ÕżČ·µÄŹĒ
A. ŌŚ±ź×¼×“æöĻĀ,1molČĪŗĪĪļÖŹµÄĢå»żĪŖ22.4L
B. ŗ¬µČĪļÖŹµÄĮæµÄČÜÖŹµÄŃĪĖįŗĶĮņĖįÖŠ,H+µÄĪļÖŹµÄĮæŅ²ĻąµČ
C. 1 mol H2ŗĶ1mol HeÖŠ,Ėłŗ¬µÄ·Ö×ÓŹżĻąĶ¬”¢Ō×ÓŹżĻąĶ¬
D. Ģå»żĪŖ6LµÄO2,ĘäÖŹĮææÉÄÜĪŖ8g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅŹ¹ÓĆpH“«øŠĘ÷Ą“²ā¶ØNa2CO3ŗĶNaHCO3»ģŗĻĪļÖŠNaHCO3µÄŗ¬Į攣³ĘČ”1.59 gѳʷ£¬ČÜÓŚĖ®Åä³É250.00 mLČÜŅŗ£¬Č”³öøĆČÜŅŗ25.00 mLÓĆ0.1 mol”¤L£1ŃĪĖį½ųŠŠµĪ¶Ø£¬µĆµ½ČēĻĀĒśĻß”£ŅŌĻĀĖµ·Ø»ņ²Ł×÷ÕżČ·µÄŹĒ( )
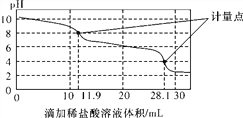
A. ÉĻŅ»øö¼ĘĮæµćĒ°·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖHCO(£«H£«===H2O£«CO2”ü
B. ĻĀŅ»øö¼ĘĮæµćČÜŅŗÖŠ“ęŌŚ“óĮæµÄŅõĄė×ÓŹĒCl£”¢HCO(
C. “Ėѳʷn(NaHCO3)£½(28.1£2”Į11.9)”Į10£4 mol
D. Ź¹ÓĆøĆ·½·Ø²ā¶ØNa2CO3ŗĶNaOH»ģŗĻČÜŅŗÖŠµÄĒāŃõ»ÆÄĘŗ¬Į棬½«»įµĆµ½1øö¼ĘĮæµć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI£®ÓŠĖÄÖÖ»ÆŗĻĪļW”¢X”¢Y”¢Z£¬ĖüĆĒŹĒÓɶĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢D”¢EÖŠµÄĮ½ÖÖŌŖĖŲ×é³É”£ŅŃÖŖ
£Ø1£©A”¢B”¢C”¢D”¢EµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĒŅA”¢DĶ¬Ö÷×壬C”¢EĶ¬Ö÷×壻B”¢C Ķ¬ÖÜĘŚ£»
£Ø2£©WÓÉA”¢B×é³É£¬Ęä·Ö×ÓÖŠŌ×ÓøöŹż±ČĪŖA£ŗB=4£ŗ1£¬³£ĪĀĪŖĘųĢ¬”£
£Ø3£©XÓÉA”¢C×é³É£¬Ęä·Ö×ÓÖŠŌ×ÓŹż±ČĪŖA£ŗC=1£ŗ1
£Ø4£©YŹĒC”¢DŠĪ³ÉµÄĄė×Ó»ÆŗĻĪļ£¬ĒŅY¾§ĢåÖŠĻąÓ¦ŌŖĖŲµÄŌ×ÓøöŹż±ČĪŖ1£ŗ1
£Ø5£©ZŹĒÓÉD”¢EŠĪ³ÉµÄĄė×Ó»ÆŗĻĪļ£¬ĘäÖŠŃōĄė×Ó±ČŅõĄė×ÓÉŁŅ»øöµē×Ó²ć£¬ŃōĄė×ÓŹżÓėŅõĄė×ÓŹżÖ®±ČĪŖ2£ŗ1 ŌņBĪŖ__________£¬WĪŖ_________£¬XµÄ½į¹¹Ź½________YµÄµē×ÓŹ½ĪŖ______________”£
II£®£Ø1£©£®Ņ»ŌŖĖŲŌ×ÓµÄN²ćÉĻÖ»ÓŠ1øöµē×Ó£¬øĆŌŖĖŲŌ×Óø÷ÄŚ²ć¾łŅŃ³äĀś£¬Š“³öøĆŌ×Óµē×ÓÅŲ¼Ź½£ŗ________________£¬
£Ø2£©Ņ»ŌŖĖŲŹōÓŚ¶ĢÖÜĘŚŌŖĖŲ£¬øĆŌŖĖŲµÄŌ×ÓŗĖĶāĖłÓŠP¹ģµĄČ«Āś»ņÕß°ėĀś£¬Š“³öøĆŌŖĖŲŌ×ӵļŪµē×Ó¹ģµĄÅŲ¼Ķ¼__________________£¬
£Ø3£©ŅŅĻ©·Ö×ÓÖŠÓŠ__________øö¦Ņ¼ü£¬___________¦Š¼ü”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com