
【题目】将等物质的量的F2和ClF混合,在密闭容器中发生反应:F2(g)+ClF(g)![]() ClF3(g) ΔH<0。下列叙述正确的是
ClF3(g) ΔH<0。下列叙述正确的是
A.保持恒容,平衡后再降低温度,平衡常数减小
B.若增加F2的用量,平衡正向移动,则反应物的转化率均增大
C.达到平衡后,若增大容器体积,则正反应速率减小,逆反应速率增大,平衡左移
D.恒温恒容时,当ClF转化40%时,容器内的压强为初始时的0.8
【答案】D
【解析】
A、正反应是放热反应,则保持恒容,平衡后再降低温度,平衡向正反应方向移动,因此平衡常数增大,A不正确;
B、若增加F2的用量,平衡正向移动,ClF的转化率增大,但单质氟的转化率降低,B不正确;
C、正反应是体积减小的可逆反应,达到平衡后,若增大容器体积,压强降低,则正反应速率和逆反应速率均减小,平衡左移,C不正确;
D、恒温恒容时,当ClF转化40%时,则
F2(g)+ClF(g)![]() ClF3(g)
ClF3(g)
起始量(mol) n n 0
转化量(mol) 0.4n 0.4n 0.4n
平衡量(mol) 0.6n 0.6n 0.4n
所以容器内的压强为初始时的![]() =0.8倍,D正确;
=0.8倍,D正确;
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】可逆反应:FeCl3+3KSCN![]() Fe(SCN)3+3KCl,离子方程式为:Fe3++3SCN-
Fe(SCN)3+3KCl,离子方程式为:Fe3++3SCN-![]() Fe(SCN)3,达到平衡后,进行下列操作,平衡怎样移动?
Fe(SCN)3,达到平衡后,进行下列操作,平衡怎样移动?
(1)加入少量FeCl3固体:平衡向____________移动;
(2)加入少量KSCN固体:平衡向____________移动;
(3)加入少量KCl固体:平衡____________移动,其理由是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是目前的主要空气污染物之一,它的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)![]() 的消除。可以用碳酸钠溶液来进行吸收,在产生
的消除。可以用碳酸钠溶液来进行吸收,在产生![]() 的同时,会生成
的同时,会生成![]() ,
,![]() 是工业盐的主要成分,在漂白、电镀等方面应用广泛。
是工业盐的主要成分,在漂白、电镀等方面应用广泛。
①写出碳酸钠溶液消除![]() 的化学方程式:________________。
的化学方程式:________________。
②写出两种能提高![]() 消除率的措施:________________。
消除率的措施:________________。
③经过一系列后续操作可以得到产品![]() ,但一般会混有一定量________的杂质。
,但一般会混有一定量________的杂质。
(2)![]() 的消除。空气中
的消除。空气中![]() 主要来自于汽车尾气的排放和硝酸工厂废气的排放,利用强氧化剂过硫酸钠(
主要来自于汽车尾气的排放和硝酸工厂废气的排放,利用强氧化剂过硫酸钠(![]() )氧化脱除
)氧化脱除![]() 可以消除污染,其流程如下:
可以消除污染,其流程如下:

①反应1的离子方程式为________________。
②反应2中![]() 的初始浓度为
的初始浓度为![]() ,反应为
,反应为![]() 。不同温度下,达到平衡时
。不同温度下,达到平衡时![]() 的脱除率与过硫酸钠(
的脱除率与过硫酸钠(![]() )初始浓度的关系如下图所示。
)初始浓度的关系如下图所示。

图中点a和点b的平衡常数K的大小关系为________________。判断依据是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图能量关系示意图,下列说法正确的是( )

A.1molC(s)与1 molO2(g)的能量之和为393.5kJ
B.反应2CO(g)+O2(g)=2CO2(g)中,生成物的总能量大于反应物的总能量
C.由C(s)→CO(g)的热化学方程式为:2C(s)+O2(g)= 2CO(g) ΔH=-221.2kJ·mol-1
D.CO的燃烧热ΔH=-282.9kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等物质的量的氧气(O2)和臭氧(O3),所含的分子数之比为___,所含的氧原子数之比为___,其相对分子量之比为___,其质量之比为___;若O2和 O3质量相等,则其分子数之比为___,氧原子数之比___。
(2)一定条件下,硝酸铵受热分解的化学方程式为:5NH4NO3═2HNO3+4N2↑+9H2O,用双线桥标出电子转移情况___。5NH4NO3═2HNO3+4N2↑+9H2O,在该反应中是氧化产物___,被氧化与被还原的N原子个数之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确的是( )
A.KClO3作氧化剂,每生成1mol [Fe(OH)SO4]n消耗![]() mol KClO3
mol KClO3
B.绿矾长时间置于空气中易被氧化
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.聚合硫酸铁与漂白粉都是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子材料在疫情防控和治疗中起到了重要的作用。下列说法正确的是
A.聚乙烯是生产隔离衣的主要材料,能使酸性高锰酸钾溶液褪色
B.聚丙烯酸树脂是3D打印护目镜镜框材料的成分之一,可以与NaOH溶液反应
C.天然橡胶是制作医用无菌橡胶手套的原料,它是异戊二烯发生缩聚反应的产物
D.聚乙二醇可用于制备治疗新冠病毒的药物,聚乙二醇的结构简式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂/氟化碳电池稳定性很高。电解质为LiClO4的乙二醇二甲醚溶液,总反应为xLi+CFx=xLiF+C,放电产物LiF沉积在正极,工作原理如图所示。下列说法正确的是

A.正极的电极反应式为CFx+xe-+xLi+=xLiF+C
B.交换膜为阴离子交换膜
C.电解质溶液可用LiClO4的乙醇溶液代替
D.b极电势高于a极电势
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用以下装置探究氯气与氨之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。
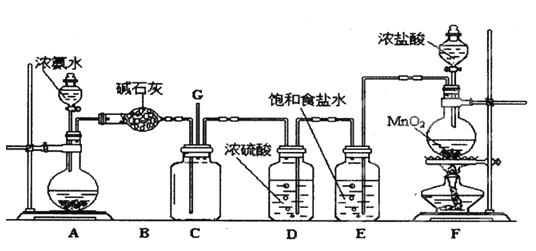
请回答下列问题:
(1)装置F中发生反应的化学方程式为____________________________.
(2)装置B中仪器的名称是___________;装置E的作用是______________________.
(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式___________________________________.
(4)装置C内当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为_______mol-1(用含a、b的代数式表示)。
(5)将用F、E、D装置制得的氯气通人含74gCa(OH)2的石灰乳中,最多可制得漂白粉_______g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com