
如图是一个制取氯气并以氯气为原料进行特定反应的装置。
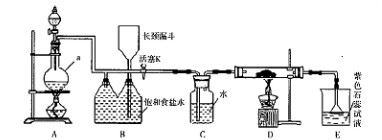
(l)A是氯气发生装置,写出其中的化学反应方程式 。
(2)a仪器的名称为 。
(3)实验开始时,先点燃A处的酒精灯,打开活塞K,让 氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HC1。写出D中反应的化学方程式 ,装置C的作用是 。
氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HC1。写出D中反应的化学方程式 ,装置C的作用是 。
(4)在E处,若漏斗内气体带有黄绿色,则紫色石蕊试液的颜色变化为 。
(5)若将E处烧杯中溶液改为澄清石灰水,反应过程中现象为 (填序号)。
①有白色沉淀生成;②无白色沉淀生成;③先生成白色沉淀,而后白色沉淀消失。
(6)D处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2
产生,则装置B中的现象是 ;若发现装置B中该现象不明显,可能的
原因是 ;查找原因时可用肥皂水或湿润的碘化钾淀粉试纸等,若用蘸
有浓氨水的玻璃棒检查时观察到有白烟产生,写出该氧化还原反应的化学方程
式 。
(1)MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)圆底烧瓶
(3)2Cl2+2H2O(气)+C  4HCl+CO2 吸收Cl2中的HCl气体,提供D处所需水蒸气
4HCl+CO2 吸收Cl2中的HCl气体,提供D处所需水蒸气
(4)由紫色变为红色,再变为无色
(5)②
(6)装置B中瓶内液面下降,长颈漏斗内液面上升; A或B装置漏气
3Cl2+8NH3═6NH4Cl+N2
【解析】(l)依据装置分析可知实验室制备氯气利用二氧化锰和浓盐酸加热反应生成;(2)根据仪器的名称判断;
(3)氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应;氯化氢气体极易溶于水,且水能提供水蒸气,据此分析;
(4)紫色石蕊试液遇酸变红,但次氯酸有漂白性,据此分析;
(5)氯化氢、次氯酸和澄清石灰水反应都生成可溶性的盐和水;
(6)根据B装置内气体的压强变化分析液面变化;若发现装置B中该现象不明显,可能是A或B装置漏气,氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种常见的气体单质,白烟为氯化铵、单质为氮气。


科目:高中化学 来源:2014高考名师推荐化学--预测6 题型:选择题
下列说法中不正确的是
A.光导纤维、硝化纤维、铜氨纤维、玻璃纤维的主成分都是糖类
B.生理盐水、葡萄糖注射液都不能产生丁达尔效应现象,不属于胶体
C.红外光谱仪可用于测定化合物的官能团、1H核磁共振仪可确定H所处的化学环境
D.用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可到达水果保鲜的目的
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测4 题型:选择题
对常温下pH=3的CH3COOH溶液,下列叙述不正确的是
A.c(H+)=c(CHCOO-)+c(OH-)
B.加入少量CH3COONa固体后,加入,c(CH3COO-)降低
C.该溶液中由水电离出的c(H+)是1.0×10-11 mol/L
D.与等体积pH =11的NaOH溶液混合后所得溶液显酸性
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
下列各组离子一定能大量共存的是
A.加入铝粉有氢气产生的溶液中Na+ 、K+ 、SO42-、Cl- 、HCO3-
B.含有大量硝酸根离子的溶液中H+ 、Fe2+ 、SO42-、Cl-
、SO42-、Cl-
C.常温下,c(H+)/c(OH-) = 1×10-10 的溶液中NH4+ 、K+ 、Ca2+ 、Cl-
D. 常温下pH=1的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
在20 mL 0.1mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是

A.溶液??性时,回滴加入适量的NaOH,溶液中离子浓度可能为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
B.C点时其pH=5.6,溶质恰好为等物质的量CH3COONa和CH3COOH,则溶液中微粒浓度关系为:c(Na+)>c(CH3COO-)
C.在B点,a>20,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在D点:c(CH3COOH)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测2 题型:选择题
下列反应的离子方程式正确的是
A.Na2CO3溶液与NaHSO4溶液反应:CO32--+2H+=CO2↑+H2O
B.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓
C.碘化钾溶液中滴入稀硫酸酸化的双氧水反应:2I-+H2O2+2H+=H2O+I2
D.海水制取溴时用纯碱吸收吹出的溴:3Br2+3H2O=5Br-+BrO3-+6H+
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:推断题
已知:
水杨酸酯E为紫外吸收剂,可用于配制防晒霜。E的一种合成路线如下:

请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%。则A的分子式为 ;结构分析显示A只有一个甲基,A的名称为 。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为 。
(3)C有 种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂 ;
(4)第③的反应类型为 ;D所含官能团的名称为 。
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式: 。
A、分子中含有6个碳原子在一条线上
B、分子中所含官能团包括水杨酸具有的官能团
(6)第④步的反应条件为 ;写出E的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:选择题
某有机物的分子式为C4H8O2,有关其同分异构体数目的说法错误的是
A.属于酯类的有4种
B.属于羧酸的有2种
C.既含有羟基又含有醛基的有3种
D.存在分子中含有六元环的同分异构体
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10,下列说法不正确的是
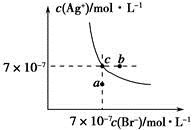
A.在t ℃时,AgBr的Ksp为4.9×10-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t ℃时,AgCl(s)+Br-(aq)  AgBr(s)+Cl-(aq)平衡常数K≈816
AgBr(s)+Cl-(aq)平衡常数K≈816
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com