
 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数(Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
分析 (1)氢氟酸是弱电解质,溶液中存在电离平衡,加水稀释其溶液促进氢氟酸电离,注意水的离子积常数只与温度有关;
(2)A.酸或碱抑制了水电离,含有弱根离子的盐促进水电离;
B.在①点时pH=6,溶液显示酸性,根据电荷守恒分析;
C.在②点时,溶液为中性,根据电荷守恒分析离子浓度大小;
D.等物质的量的氢氟酸和氢氧化钠恰好反应生成氟化钠,溶液呈碱性,根据电荷守恒判断,注意等体积混合时,不水解离子浓度变为原来的一半;
(3)等物质的量浓度的钠盐溶液,酸根离子水解程度越大其溶液的pH越大;
(4)设计实验使溶液中的CO32-由有到无,再根据酚酞的颜色变化起作用的是否是碳酸根离子;
(5)根据原子守恒确定A,再根据化合价变化计算转移电子.
解答 解:(1)氢氟酸是弱电解质,溶液中存在电离平衡,加水稀释其溶液促进氢氟酸电离,
A.稀释过程中促进氢氟酸电离,但c(H+)减小,故A错误;
B.温度不变,水的离子积常数不变,所以c(H+)•c(OH-)不变,故B错误;
C.稀释过程中促进氢氟酸电离,氢离子个数增大,氟化氢分子个数减小,所以 $\frac{c({H}^{+})}{c(HF)}$ 增大,故C正确;
D.稀释过程中促进氢氟酸电离,溶液的体积增大程度大于氢离子的物质的量,所以氢离子浓度降低,氢氧根离子浓度增大,则$\frac{c(O{H}^{-})}{c({H}^{+})}$增大,故D正确;
故答案为:CD;
(2)A.氢氟酸抑制水电离,氟化钠促进水电离,所以pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)不相等,故A错误;
B.①点时pH=6,溶液中存在电荷守恒,c(F-)+c(OH-)=c(Na+)+c(H+),所以c(F-)-c(Na+)=c(H+)-c(OH-)=9.9×10-7mol/L,故B正确;
C.②点时,溶液呈中性,c(OH-)=c(H+),溶液中存在电荷守恒,c(F-)+c(OH-)=c(Na+)+c(H+),所以c(F-)=c(Na+),故C正确;
D.③点时V=20mL,此时溶液中溶质在氟化钠,溶液呈碱性,根据电荷守恒知c(F-)<c(Na+),但等体积混合时不水解的离子浓度变为原来的一半,所以c(F-)<c(Na+)=0.05mol/L,故D错误;
故答案为:BC;
(3)等物质的量浓度的钠盐溶液,酸根离子水解程度越大其溶液的pH越大,酸的电离常数越小其酸根离子水解程度越大,所以等物质的量浓度的①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液中pH由大到小的顺序是①④②③,
故答案为:①④②③;
(4)为证明纯碱溶液呈碱性是由CO32-引起的,就设计一个使溶液中的碳酸根离子由有到无的实验,根据溶液中酚酞颜色的变化判断,所以设计的实验为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅,则说明Na2CO3溶液显碱性是因为CO32-水解的缘故,
故答案为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅;
(5)根据原子守恒知,该反应方程式为:HFO+H2O=HF+H2O2,根据元素化合价知,每生成1molHF转移 1mol电子,故答案为:1.
点评 本题考查较综合,涉及弱电解质的电离、盐类水解、实验设计、氧化还原反应等知识点,注意(3)中D选项,等体积混合时,不水解的离子其浓度变为原来的一半,明确HOF中各元素的化合价,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 面粉和食盐的混合物 | B. | 石灰石与泥沙的混合物 | ||
| C. | 碘与酒精的混合物 | D. | 泥沙与氯化钠的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 使用药品 | 现象 |
| Ⅰ | Na2O2、H2O | ①试管壁发热 ②有无色无味气体产生 |
| Ⅱ | Na2O2、浓盐酸 | ①试管壁发热 ②有刺激性气味的气体产生 ③反应后所得溶液呈浅黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
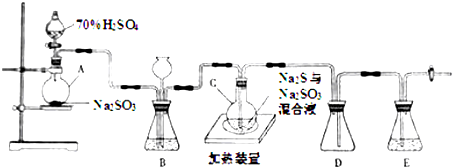
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铜溶液 | B. | 0.5mol•L-1盐酸 | C. | 0.5mol•L-1H2SO4 | D. | 自来水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直径介于1--10nm之间的粒子称为胶体 | |
| B. | 利用丁达尔效应可以区别溶液与胶体 | |
| C. | 氢氧化铁胶体是纯净物 | |
| D. | 可以通过过滤的方法分离胶体和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物电离时,生成的阴离子有氢氧根离子的是碱 | |
| B. | 在相同温度下,强电解质溶液一定比弱电解质溶液的导电性强 | |
| C. | 碱性氧化物都是金属氧化物,正盐中可能含有氢元素 | |
| D. | 向醋酸溶液中加入少量氢氧化钠溶液,因发生中和反应,溶液的导电能力降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质(少量) | 试剂和操作方法 | |
| A | O2 | H2O(蒸汽) | 通过浓H2SO4 |
| B | CO2 | CO | 点燃 |
| C | KCl固体 | KClO3 | 加入MnO2并加热 |
| D | KNO3溶液 | Ba(NO3)2溶液 | 加入适量的Na2SO4溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com