
| A. | 制作印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | Ca(HCO3)2溶液中加足量NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 硫酸镁溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| D. | KClO3溶液与浓盐酸反应:ClO3-+5Cl-+6H+═3Cl2↑+3H2O |
分析 A.电荷不守恒;
B.氢氧化钠足量,反应生成碳酸 钙、碳酸钠和水;
C.漏掉镁离子与氢氧根离子的反应;
D.二者发生氧化还原反应生成氯化钾、氯气和水.
解答 解:A.制作印刷电路板,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.Ca(HCO3)2溶液中加足量NaOH溶液,离子方程式:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32-,故B错误;
C.硫酸镁溶液与氢氧化钡溶液反应,离子方程式:Mg2++2OH-+SO42-+Ba2+═BaSO4↓+Mg(OH)2↓,故C错误;
D.KClO3溶液与浓盐酸反应,离子方程式:ClO3-+5Cl-+6H+═3Cl2↑+3H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应遵循客观事实、遵循电荷守恒、原子个数守恒规律,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- | |
| B. | 含有大量OH-的溶液:Na+、Ca2+、SO42-、CO32- | |
| C. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| D. | 含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl-和37Cl-离子结构示意图均可以表示为: | |
| B. | HClO的结构式:H-Cl-O | |
| C. | HF的电子式: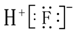 | |
| D. | 质子数为92、中子数为146的U原子:14692U |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地下钢管连接锌板属于牺牲阳极的阴极保护法 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 化学平衡发生移动,平衡常数一定发生改变 | |
| D. | 强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
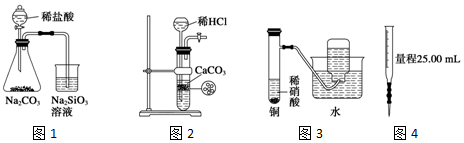
| A. | 图1为证明非金属性强弱:Cl>C>Si | |
| B. | 图2为制备少量CO2并控制反应 | |
| C. | 图3为制备并收集少量NO气体 | |
| D. | 图4量取0.10mol•L-1 KOH溶液20.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4═H2++SO42- | B. | Ba(OH)2═Ba2++OH- | ||
| C. | NH4NO3═NH4++NO3- | D. | 2KClO3═2K++2Cl-+3O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃煤电厂的废气随意排放 | |
| B. | 采暖燃煤锅炉安装脱硝等净化设施 | |
| C. | 尽量步行或骑自行车出行 | |
| D. | 重污染工业企业持续推进能源结构调整 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com