
下表为元素周期表的—部分,请参照元素①一⑨在表中的位置,回答下列问题。
| 族
| IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)第三周期中元素非金属性最强的元素的原子结构示意图是___________。
(2)②③⑦最高价氧化物对应水化物酸性由强到弱的顺序是___________(填化学式)。
(3)用电子式表示③的氢化物:_________________________________。
(4)下列可以判断⑤和⑥金属性强弱的是______________________(填序号)。
a. 单质的熔点⑤比⑥低 b. 化合价⑤比⑥低
c. 单质与水反应⑤比⑥剧烈 d. 最高价氧化物的水化物的碱性⑤比⑥强
(5)含有上述元素的物质间存在以下转化:
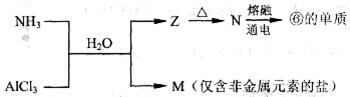
a. Z的化学式是___________。
b. N生成⑥的单质反应的化学方程式是_________________________________。
科目:高中化学 来源: 题型:
常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A.1∶9 B.1∶1 C.1∶2 D.1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:① 称取一定质量的HA配制0.lmol/L的溶液100mL;
② 用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:① 用已知物质的量浓度的HA溶液、盐酸,分别配制pH=l的两种酸溶液各100mL;
② 分别取这两种溶液各10mL,加水稀释为100mL;
③ 各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)用pH试纸测定HA溶液pH的操作方法为 。
(3)甲方案中,说明HA是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
(4)乙方案中,说明HA是弱电解质的现象是 (选填编号)。
(a)装HCl溶液的试管中放出H2的速率快;
(b)装HA溶液的试管中放出H2的速率快;
(c)两个试管中产生气体速率一样快。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置不能达到实验目的的是 ( )
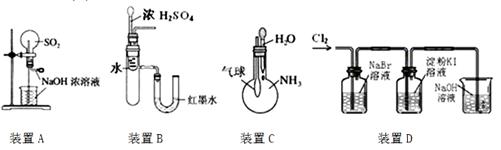
A.用装置A来做SO2的喷泉实验
B.用装置B来验证浓H2SO4与水混合的热量变化
C.用装置C来验证NH3易溶于水
D.用装置D来验证氧化性:Cl2>Br2>I2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列涉及的有机物及有机反应类型正确的是 ( )。
A.乙烯分子与苯分子中的碳碳键不同,但二者都能发生加成反应
B.除去甲烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶
C.苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环结构
D.乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下1.68 L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水中,得到的白色沉淀质量为15.0 g;若用足量碱石灰吸收燃烧产物,质量增加9.3 g。
(1)燃烧产物中生成水的质量是_______________________________ _________________________________________。
(2)若原气体是单一气体,则它的分子式是_____________________。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出两组)____________________________ ____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验探究:探究碳、硅元素的非金属性的相对强弱,根据要求完成下列各小题:
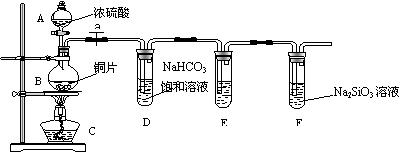 (1)实验装置:
(1)实验装置:
填写所示仪器名称A ; B
(2)实验步骤:
连接仪器、_____________、加药品后,打开a、然后滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是 ;
装置E中足量酸性KMnO4溶液(具有强氧化性)的作用是 ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性_ __ (填“能”或“否”),试管D中发生反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1 NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法不正确的是( )
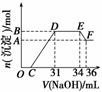
A.OC段反应离子方程式:H++OH-===H2O
B.溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+
C.溶液中n(NH )=0.012 mol
)=0.012 mol
D.欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com