
| A、水晶是无色透明的晶体,可用制作硅太阳能电池 |
| B、配制0.1mol/L NaCl溶液,若定容时俯视,则所得溶液浓度偏小(其它操作均正确) |
| C、向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积不变 |
| D、已知:(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9 kJ?mol-1,因此该反应一定不能自发进行 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀,说明浓硫酸具有脱水性和强氧化性 |
| B、Fe与浓硫酸由于温度不同而能发生不同氧化还原反应 |
| C、Ba(NO3)2溶液分别滴入Na2SO3和Na2SO4溶液中均能生成沉淀,但沉淀不是同一种物质 |
D、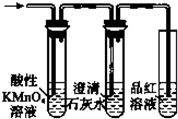 用如图装置检验乙烯中混有SO2和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、饱和氯化铁溶液滴加沸水中:Fe3++3H2O=Fe(OH)3↓+3H+ | ||
B、CO2通入过量的NaOH溶液:CO2+OH-═HCO
| ||
| C、大理石溶于硝酸:CaCO3+2H+═Ca2++CO2↑+H2O | ||
| D、碳酸钡和稀硫酸:BaCO3+2H+═Ba2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、④③②① |
| C、③④②① | D、②③④① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、K+、Na+、SO42- |
| B、Na+、K+、CO32-、Cl- |
| C、Mg2+、Na+、Cl-、NO3- |
| D、Ba2+、K+、HCO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(OH-)>c(HS-)>c(S2-) |
| B、c(Na+)+c(H+)=c(HS-)+c(S2-)+c(OH-) |
| C、2c(Na+)=c(H2S)+c(HS-)+c(S2-) |
| D、c(OH-)=c(H+)+2c(H2S)+c(HS-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com