
·ÖĪö £Ø1£©¢ŁH2£Øg£©+X£Øl£©ØTY£Øl£©”÷H1£¬¢ŚO2£Øg£©+Y£Øl£©ØTX£Øl£©+H2O2£Øl£©”÷H2£¬Į½·“Ó¦µÄ”÷S£¼0£¬Į½·“Ó¦¾łĪŖ×Ō·¢·“Ó¦£¬øł¾Ż”÷G=”÷H-T”÷S£¼0½įŗĻøĒĖ¹¶ØĀÉÅŠ¶Ļ£»
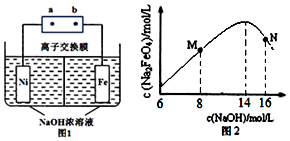
£Ø2£©¾ŻNaBH4ŹĒŅ»ÖÖÖŲŅŖµÄ“¢ĒāŌŲĢ壬ÄÜÓėĖ®·“Ӧɜ³ÉNaBO2£¬ĒŅ·“Ó¦Ē°ŗóBµÄ»ÆŗĻ¼Ū²»±ä£¬æÉÖŖHŌŖĖŲ»ÆŗĻ¼ŪÓÉ-1¼Ū”¢+1¼Ū±äĪŖ0¼Ū£¬ŌŁ½įŗĻ×ŖŅʵē×ÓŹŲŗćŹéŠ“»Æѧ·½³ĢŹ½£»£Ø3£©¢Łµē½ā³ŲÖŠŃō¼«·¢ÉśŃõ»Æ·“Ó¦£¬ŅĄ¾ŻĢāŅāæÉÖŖĢśŌŚŃō¼«Ź§Č„µē×Ó£¬¼īŠŌ»·¾³ĻĀÉś³ÉøßĢśĖįøłĄė×Ó£¬ĖłŅŌÓėĘäĻąĮ¬µÄŅ»¼«ŹĒÕż¼«£¬ĮķŅ»¼«ŹĒøŗ¼«£»¾Ż“ĖŹéŠ“µē¼«·“Ó¦Ź½£»
¢Śøł¾ŻĢāŅāÄųµē¼«ÓŠĘųÅŻ²śÉśŹĒĒāĄė×ӷŵēÉś³ÉĒāĘų£¬Ģśµē¼«·¢ÉśŃõ»Æ·“Ó¦£¬ČÜŅŗÖŠµÄĒāŃõøłĄė×Ó¼õÉŁ£¬Ņņ“Ėµē½āŅ»¶ĪŹ±¼äŗó£¬c£ØOH-£©½µµĶµÄĒųÓņŌŚŃō¼«ŹŅ£»
¢Ūøł¾ŻĢāŅāNa2FeO4Ö»ŌŚĒæ¼īŠŌĢõ¼žĻĀĪČ¶Ø£¬ŌŚMµć£¬c£ØOH-£©µĶ£¬Na2FeO4ĪČ¶ØŠŌ²ī£¬ĒŅ·“Ó¦Āż£¬ŌŚNµć£ŗc£ØOH-£©¹żøߣ¬Ģśµē¼«ÉĻÓŠĒāŃõ»ÆĢśÉś³É£¬Ź¹Na2FeO4²śĀŹ½µµĶ£®
½ā“š ½ā£ŗ£Ø1£©¢ŁH2£Øg£©+X£Øl£©ØTY£Øl£©”÷H1£¬¢ŚO2£Øg£©+Y£Øl£©ØTX£Øl£©+H2O2£Øl£©”÷H2£¬Į½·“Ó¦µÄ”÷S£¼0£¬øł¾Ż”÷G=”÷H-T”÷S£¬ŅņĪŖ¾łĪŖĮ½·“Ó¦×Ō·¢·“Ó¦£¬Ņņ“Ė”÷H¾łŠ”ÓŚ0£¬øł¾ŻøĒĖ¹¶ØĀɽ«¢Ł+¢ŚµĆ£ŗH2£Øg£©+O2£Øg£©=H2O2£Øl£©µÄ”÷H=”÷H1+”÷H2£¼0£¬
¹Ź“š°øĪŖ£ŗ×Ō·¢·“Ó¦ŠčĀś×ć”÷G=”÷H-T”÷S£¼0£¬Ōņ”÷H1£¼0”¢”÷H2£¼0£¬øł¾ŻøĒĖ¹¶ØĀÉ”÷H=”÷H1+”÷H2£¼0£»
£Ø2£©NaBH4ŹĒŅ»ÖÖÖŲŅŖµÄ“¢ĒāŌŲĢ壬ÄÜÓėĖ®·“Ӧɜ³ÉNaBO2£¬ĒŅ·“Ó¦Ē°ŗóBµÄ»ÆŗĻ¼Ū²»±ä£¬ĖłŅŌNaBH4ÓėH2O·¢Éś¹éÖŠ·“Ó¦£¬Éś³ÉNaBO2ŗĶĒāĘų£¬HŌŖĖŲ»ÆŗĻ¼ŪÓÉ-1¼Ū”¢+1¼Ū±äĪŖ0¼Ū£¬ŅĄ¾ŻµĆŹ§µē×ÓŹŲŗćæÉÖŖ£ŗNaBH4µÄĻµŹżĪŖ1£¬H2OµÄĻµŹżĪŖ2£¬ŅĄ¾ŻŌ×ÓøöŹżŹŲŗć£¬·“Ó¦·½³ĢŹ½£ŗNaBH4+2H2O=NaBO2+4H2”ü£»
¹Ź“š°øĪŖ£ŗNaBH4+2H2O=NaBO2+4H2”ü£»
£Ø3£©¢Łµē½ā³ŲÖŠŃō¼«·¢ÉśŃõ»Æ·“Ó¦£¬ŅĄ¾ŻĢāŅāæÉÖŖĢśŌŚŃō¼«Ź§Č„µē×Ó£¬¼īŠŌ»·¾³ĻĀÉś³ÉøßĢśĖįøłĄė×Ó£¬µē¼«·“Ó¦Ź½ĪŖ£ŗFe-6e-+8OH-=FeO42-+4H2O£»
øł¾ŻĢāŅāÄųµē¼«ÓŠĘųÅŻ²śÉśŹĒĒāĄė×ӷŵēÉś³ÉĒāĘų£¬Ģśµē¼«·¢ÉśŃõ»Æ·“Ó¦£¬ÓėµēŌ“µÄøŗ¼«ĻąĮ¬£¬
¹Ź“š°øĪŖ£ŗøŗ£»Fe-6e-+8OH-ØTFeO+4H2O£»
¢Śøł¾ŻĢāŅāÄųµē¼«ÓŠĘųÅŻ²śÉśŹĒĒāĄė×ӷŵēÉś³ÉĒāĘų£¬Ģśµē¼«·¢ÉśŃõ»Æ·“Ó¦£¬ČÜŅŗÖŠµÄĒāŃõøłĄė×Ó¼õÉŁ£¬Ņņ“Ėµē½āŅ»¶ĪŹ±¼äŗó£¬c£ØOH-£©½µµĶµÄĒųÓņŌŚŃō¼«ŹŅ£¬c£ØOH-£©ÉżøßµÄĒųÓņŌŚŅõ¼«ŹŅ£¬
¹Ź“š°øĪŖ£ŗŅõ¼«ŹŅ£»
¢Ūøł¾ŻĢāŅāNa2FeO4Ö»ŌŚĒæ¼īŠŌĢõ¼žĻĀĪČ¶Ø£¬ŌŚMµć£¬c£ØOH-£©µĶ£¬Na2FeO4ĪČ¶ØŠŌ²ī£¬ĒŅ·“Ó¦Āż£¬ŌŚNµć£ŗc£ØOH-£©¹żøߣ¬Ģśµē¼«ÉĻÓŠĒāŃõ»ÆĢśÉś³É£¬Ź¹Na2FeO4²śĀŹ½µµĶ£»
¹Ź“š°øĪŖ£ŗc£ØOH-£©µĶ£¬Na2FeO4ĪČ¶ØŠŌ²ī£¬ĒŅ·“Ó¦Āż£»c£ØOH-£©¹żøߣ¬Ģśµē¼«ÉĻÓŠĒāŃõ»ÆĢśÉś³É£¬Ź¹Na2FeO4²śĀŹ½µµĶ£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦µÄ·½Ļņ”¢·“Ó¦·½³ĢŹ½µÄŹéŠ“”¢µē»ÆѧµČÖŖŹ¶£¬²ąÖŲæ¼²éĮĖµē½ā·ØÖĘČ”Na2FeO4£¬Ć÷Č·”÷G=”÷H-T”÷S£¼0ÅŠ¶Ļ·“Ó¦·½Ļņ”¢ŹģĮ·ÕĘĪÕøĒĖ¹¶ØĀÉŅŌ¼°µē½ā³Ų¹¤×÷ŌĄķ¼°µē¼«·“Ó¦Ź½µÄŹéŠ“·½·ØŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ±£»¤øÖĢśĖ®Õ¢ĆÅæÉÓĆĶā½ÓµēŌ“Ńō¼«±£»¤·Ø | |
| B£® | ·“Ó¦NH3£Øg£©+HI£Øg£©ØTNH4I£Øs£©ŌŚµĶĪĀĻĀæÉ×Ō·¢½ųŠŠ£¬Ōņ”÷H£¾0£¬”÷S£¾0 | |
| C£® | ³£ĪĀĻĀ£¬Ļņ0£®lmol•L-1CH3COONaČÜŅŗÖŠµĪ¼ÓŃĪĖį£¬ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČŌö“ó | |
| D£® | ŗćĪĀĻĀ½ųŠŠµÄ·“Ó¦2NO2£Øg£©?N2O4£Øg£©“ļĘ½ŗāŹ±£¬ĖõŠ”ČŻĘ÷Ģå»żŌŁ“ļĘ½ŗāŹ±£¬ĘųĢå µÄŃÕÉ«±ČµŚŅ»“ĪĘ½ŗāŹ±µÄÉī |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃéÄæµÄ | ŹµŃé²Ł×÷ | |
| A | ÖĘČ”ŅŅĖįŅŅõ„£¬ĢįøßĘ䊧ĀŹ | ¼ÓČČ£¬½«ŅŅĖįŅŅõ„Õō³ö |
| B | ±Č½ĻMg”¢AlµÄ½šŹōŠŌ | ·Ö±š½«“ņÄ„¹żµÄĆ¾“ų”¢ĀĮʬ·ÅČė·ŠĖ®ÖŠ |
| C | ōĒ»łÓ°ĻģÓėĘäĻąĮ¬µÄ±½»·»īŠŌ | ·Ö±š½«±„ŗĶäåĖ®µĪČė±½ŗĶ±½·ÓČÜŅŗÖŠ |
| D | ÖʱøFe2O3¹ĢĢå | ½«H2O£Øg£©ĶØČė×°ÓŠĢś·ŪµÄŹŌ¹Ü£¬¼ÓČČ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻąĶ¬Ģõ¼žĻĀ£¬1molCH4ŗĶ2molCH4µÄČ¼ÉÕČČ²»Ķ¬£¬ŗóÕߏĒĒ°ÕßµÄ2±¶ | |
| B£® | ¶ŌÓŚŅ»øöČ·¶ØµÄ·“Ó¦£¬·“Ó¦ČȵēóŠ”Óė·“Ó¦Ā·¾¶ÓŠ¹Ų | |
| C£® | ¶ŌÓŚ·“Ó¦CaCO3£Øs£©ØTCaO£Øs£©+CO2£Øg£©”÷H=+178.2kJ/mol£¬ŌŚøßĪĀĻĀ²ÅÄÜ·¢Éś·Ö½ā£¬ĖµĆ÷ÄÜĮæ±ä»ÆŹĒĪļÖŹ±ä»ÆµÄ»ł“” | |
| D£® | »ÆŃ§Ę½ŗā³£Źż£ØK£©µÄ“óŠ”·“Ó³ĮĖ»Æѧ·“Ó¦½ųŠŠµÄ³Ģ¶Č£¬KÖµŌ½“󣬷“Ó¦ĪļµÄ×Ŗ»ÆĀŹŌ½øß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
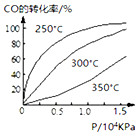 ŃŠ¾æNO2”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮
ŃŠ¾æNO2”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
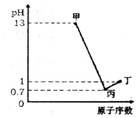 X”¢Y”¢Z”¢WĪŖĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·Ö±šĪŖ¼×”¢ŅŅ”¢±ū”¢¶”£¬³£ĪĀĻĀ¼×”¢±ū”¢¶”¾łæÉÓėŅŅ·“Ӧɜ³ÉŃĪŗĶĖ®£¬X”¢Z”¢WµÄŌ×ÓŠņŹż¼°0.1mol/L¼×”¢±ū”¢¶”ČÜŅŗµÄpHČēĶ¼ĖłŹ¾£ØŅŃÖŖlg2=0.3£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
X”¢Y”¢Z”¢WĪŖĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·Ö±šĪŖ¼×”¢ŅŅ”¢±ū”¢¶”£¬³£ĪĀĻĀ¼×”¢±ū”¢¶”¾łæÉÓėŅŅ·“Ӧɜ³ÉŃĪŗĶĖ®£¬X”¢Z”¢WµÄŌ×ÓŠņŹż¼°0.1mol/L¼×”¢±ū”¢¶”ČÜŅŗµÄpHČēĶ¼ĖłŹ¾£ØŅŃÖŖlg2=0.3£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ¼ņµ„ŅõĄė×ӵĻ¹ŌŠŌ£ŗZ£¼W | |
| B£® | X”¢Y·Ö±šÓėWŠĪ³ÉµÄ»ÆŗĻĪļ½ŌĪŖĄė×Ó»ÆŗĻĪļ | |
| C£® | ŅŅ¹ĢĢåÖŠ¼ÓČė¼×µÄČÜŅŗ»ņÅØ°±Ė®£¬¹ĢĢ嶼ÄÜČܽā | |
| D£® | Y”¢ZµÄ¼ņµ„Ąė×Ó¶¼»įÓ°ĻģĖ®µÄµēĄėĘ½ŗā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×ÓŹ½ĪŖC4H8µÄĪļÖŹŠŌÖŹ¾łÓė2-¶”Ļ©ĻąĶ¬ | |
| B£® | Ńõ»ÆŠŌ£ŗO3£¾O2 | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬22.4LµÄ2-¶”Ļ©ÖŠŗ¬C-H¼üŹżÄæĪŖ8”Į6.02”Į1023øö | |
| D£® | 1molO3²ĪÓėøĆ·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ6”Į6.02”Į1023øö |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com