
 乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.以下是一种制备乳酸亚铁的实验方法.
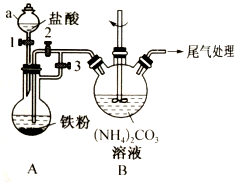
乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.以下是一种制备乳酸亚铁的实验方法.分析 制备碳酸亚铁::由装置可知,A中为盐酸与铁粉反应生成氯化亚铁和氢气的反应,Fe+2H+=Fe2++H2↑,实验时,要先后打开活塞1、活塞3-段时间,使反应发生生成的氢气赶走装置中的空气,防止生成的亚铁离子被氧化,然后关闭活塞3,打开活塞2,生成的氢气使A中气压增大,将生成的氯化亚铁压如B中与碳酸铵发生反应生成碳酸亚铁,Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,据此分析(1)~(4);
制备乳酸亚铁:
(5)FeCO3与乳酸CH3CH(OH)COOH反应生成CH3CH(OH)COO]2Fe、二氧化碳气体和水,据此写出反应的离子方程式;
(6)加入少量的铁粉是为了防止FeCO3溶解时Fe2+被氧化;
(7)从溶液中获得晶体,应经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作;
(8)先加入硫氰化钾溶液,溶液不变色,然后加入新制氯水,若溶液变为血红色则证明溶液中含有亚铁离子.
解答 解:(1)由装置构造可知仪器a为分液漏斗;A中为盐酸与铁粉反应生成氢气和氯化亚铁的反应,可观察到铁粉逐渐溶解,有气泡冒出,溶液变成浅绿色;
故答案为:分液漏斗;有气泡冒出,溶液变成浅绿色;
(2)实验时,要先后打开活塞1、活塞3-段时间,使反应发生生成的氢气赶走装置中的空气,防止生成的亚铁离子被氧化;
故答案为:引发反应产生氢气,排出装置内的空气;
(3)关闭活塞3,打开活塞2,生成的氢气使A中气压增大,将生成的氯化亚铁压如B中与碳酸铵发生反应生成碳酸亚铁;
故答案为:关闭活塞3,打开活塞2;
(4)A中的反应为Fe+2H+=Fe2++H2↑,B中的反应为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,故尾气为H2、CO2;
故答案为:H2、CO2;
(5)FeCO3与乳酸反应的化学方程式为:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O,则反应的离子方程式为:FeCO3+2CH3CH(OH)COOH=2CH3CH(OH)COO-+Fe2++CO2↑+H2O;
故答案为:FeCO3+2CH3CH(OH)COOH=2CH3CH(OH)COO-+Fe2++CO2↑+H2O;
(6)制备乳酸亚铁过程中加入Fe粉,可防止FeCO3溶解时Fe2+被氧化;
故答案为:防止FeCO3溶解时Fe2+被氧化;
(7)从乳酸亚铁溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气低温蒸发、冷却结晶、过滤、洗涤、干燥等操作,
故答案为:冷却结晶;
(8)证明乳酸亚铁中含Fe2+的方法为:取少量乳酸亚铁溶液于试管中,先滴加几滴KSCN溶液,溶液不变色,再滴加新制氯水,溶液变成血红色,
故答案为:取少量乳酸亚铁溶液于试管中,先滴加几滴KSCN溶液,溶液不变色,再滴加新制氯水,溶液变成血红色.
点评 本题考查了制备方案的设计,为高考常见题型,明确实验目的及化学实验基本操作方法为解答关键,注意掌握物质制备方案的设计与评价原则,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力,难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 纯盐酸 | 淀粉溶液 | 硫酸 | 液氨 |
| B | 漂粉精 | 水玻璃 | 氧化铝 | 二氧化硫 |
| C | 胆矾 | 氢氧化铁胶体 | 碳酸钠 | 乙醇 |
| D | 水银 | 澄清石灰水 | 氯化铜 | 铁 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
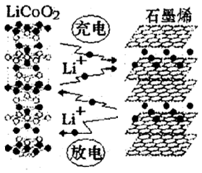 2016年12月1日,华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2 $?_{充电}^{放电}$C6+LiCoO2,其工作原理如图.下列关于该电池的说法正确的是( )
2016年12月1日,华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2 $?_{充电}^{放电}$C6+LiCoO2,其工作原理如图.下列关于该电池的说法正确的是( )| A. | 该电池若用隔膜可选用质子交换膜 | |
| B. | 放电时,LiCoO2极发生的电极反应为:LiCoO2-xe-═Li1-xCoO2+xLi+ | |
| C. | 石墨烯电池的优点是提高电池的储铿容量进而提高能量密度 | |
| D. | 废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸与氢氧化钾溶液反应:H++OH-═H2O | |
| B. | 过氧化钠与水反应:2Na2O 2+2H2O═4Na++4OH-+O2↑ | |
| C. | 氧化铁溶于盐酸:Fe2O3+6H+═2Fe3++3H2O | |
| D. | Na与硫酸铜溶液反应:2Na+Cu2+═2Na++Cu |
查看答案和解析>>
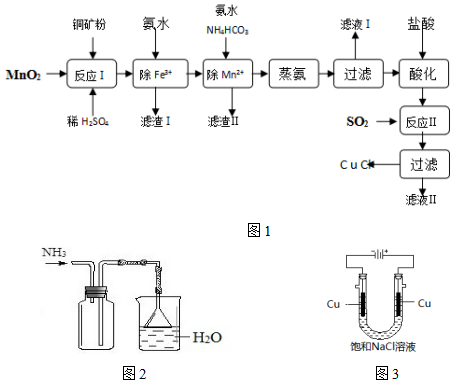
科目:高中化学 来源: 题型:解答题
| 序号 | 温度/℃ | 时间/min | 压强/KPa | 残液颜色 |
| a | 110 | 60 | 101.3 | 浅蓝色 |
| b | 100 | 40 | 74.6 | 几乎很浅 |
| c | 90 | 30 | 60.0 | 无色透明 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+2HCl═FeCl2+H2 | B. | CH4$\frac{\underline{\;高温\;}}{\;}$C+2H2 | ||
| C. | Mg(OH)2+2HCl═MgCl2+2H2O | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水放在棕色试剂瓶中,避光保存 | |
| B. | 液溴密封盛放在棕色瓶中,液面上放一层水 | |
| C. | 少量金属钠保存在四氯化碳中 | |
| D. | 水玻璃保存在带胶塞的玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 皂化反应的产物是高级脂肪酸和甘油 | |
| B. | 酯化反应和酯的水解反应均为取代反应 | |
| C. | 将苯与浓溴水混合可制取溴苯 | |
| D. | 新戊烷和2-甲基丁烷是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
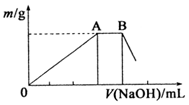 铝及其化合物在生产和生活等方面有广泛的应用.请回答下列问题:
铝及其化合物在生产和生活等方面有广泛的应用.请回答下列问题: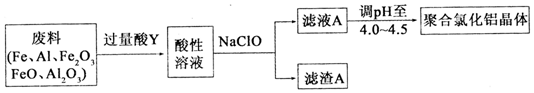
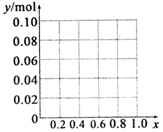
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com