
为了比较铁和铜金属活动性强弱,某研究小组的同学设计了如下一些方案,并将实验结果记录如下:
| 方案 | 现象或产物 |
| |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| |
| ②将铁丝和铜丝分别在氯气中燃烧 | 产物分别为FeCl3和CuCl2 |
| |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和CuSO4 |
| |
| ④将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡,铜片上不产生气泡 |
| |
| ⑤将铁片和铜片同时插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 | ||
能根据以上各种现象或产物证明铁的金属活动性比铜强的方案一共有( )。
A.2种 B.3种
C.4种 D.5种
科目:高中化学 来源: 题型:
下列说法正确的是( )
①有化学键破坏的变化一定属于化学变化 ②发生颜色变化的一定是化学变化 ③电解的过程一定发生化学变化 ④用糯米、酒曲和水制成甜酒酿,一定是化学变化
A.①③ B.②③④ C.③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响 ,实验结果如下图所示(注:T1、T2均大于300 ℃):
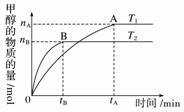
下列说法正确的是____(填序号)。
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为
v(CH3OH)=mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时增大
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
在100℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:[2NO2(g)  N2O4(g) ΔH<0]
N2O4(g) ΔH<0]
| 容器 | 物质 | 起始浓度/(mol·L-1) | 平衡浓度/(mol·L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
下列说法正确的是
A. 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2)
B. 平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ) = 2K(Ⅱ)
C. 平衡后,升高相同温度,以N2O4表示的反应速率ν(Ⅰ)<ν(Ⅱ)
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属元素的叙述正确的是( )
A.金属元素的单质只有还原性,其离子只有氧化性
B.金属元素的单质在常温下均为固体
C.金属元素在不同化合物中化合价均相同
D.大多数金属元素的单质为电的良导体
查看答案和解析>>
科目:高中化学 来源: 题型:
随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”。为回收利用含钒催化剂(含有V2O15、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上。部分含钒物质在水中的溶解性如表所示:
| 物质 | VOSO4 | V2O15 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
该工艺的主要流程如下。
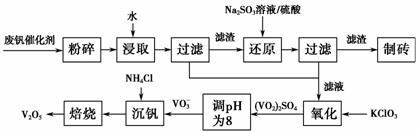
请回答下列问题:
(1)请写出加入Na2SO3溶液发生反应的离子方程式
________________________________________________________________________。
(2)催化氧化所使用的催化剂钒触媒(V2O15)能加快二氧化硫的氧化速率,此过程中产生了一连串的中间体(如图1)。其中a、c两步的化学方程式可表示为________________________,________________________________。
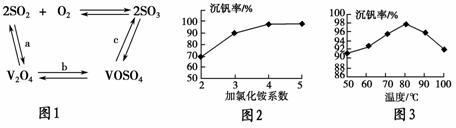
(3)该工艺中沉钒率是回收钒的关键之一,沉钒率的高低除受溶液pH影响外,还需要控制氯化铵的系数(NH4Cl加入质量与料液中V2O15的质量比)和温度。根据图2和图3,试建议控制氯化铵系数和温度的适宜值分别为________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )
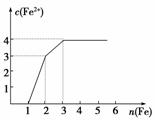
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种元素的基态原子的电子排布式如下:
①1s22s2 2p63s23p4;②1s22s22p63s23p3;
③1s22s2 2p3;④1s22s22p5。
则下列有关比较中正确的是 ( )。
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>③>②>①
D.最高正化合价:④>③=②>①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com