
| 反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| c(N2O)/mol•L-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 |
| 反应时间/min | 60 | 70 | 80 | 90 | 100 | |
| c(N2O)/mol•L-1 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
| A. | 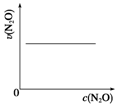 | B. |  | C. | 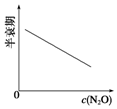 | D. |  |
分析 A.物质的浓度与速率呈正比,单位时间内变化量为定值;
B.有表中数据可知最终N2O完全分解;
C.不同浓度的半衰期不同,曲线斜率应发生变化,不是直线;
D.N2O的起始浓度越小,有利于平衡正向移动,单位时间内的转化率越大.
解答 解:A.由表可知,每隔10min,c(N2O)的变化量相等,故单位时间内c(N2O)的变化量是定值,即N2O的分解速率是定值,故A正确;
B.由表可知,每隔10min,c(N2O)的变化量相等,故单位时间内c(N2O)的变化与N2O的起始浓度无关,最终N2O完全分解,故B错误;
C.0-50min,c(N2O)由0.1变为0.05,故0.1mol•L-1N2O的半衰期为50min,20-60min,c(N2O)由0.08变为0.04,故0.08mol•L-1N2O的半衰期为40min,故随着浓度的减小,半衰期也在减小,曲线斜率应发生变化,不是直线,故C错误;
D.由表可知,每隔10min,c(N2O)的变化量相等,故N2O的起始浓度越小,单位时间内的转化率越大,最终N2O完全分解,故D错误,
故选A.
点评 本题考查平衡图象分析,为高频考点,侧重考查学生的分析能力,难度中等,该题所给图表、图象新颖,信息量大,但给出了半衰期的注释,降低了难度,有利于学生答题.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:多选题
| A. | 向SO2水溶液中加入少量NaHCO3粉末,有气泡产生,说明H2SO3酸性强于H2CO3 | |
| B. | 向SO2水溶液中滴加Ba(NO3)2溶液,有白色沉淀产生,说明SO2水溶液中含有SO42- | |
| C. | 向SO2水溶液中通入H2S气体,有淡黄色沉淀产生,说明SO2水溶液具有氧化性 | |
| D. | 向KMnO4溶液中滴加SO2水溶液,溶液颜色褪去,说明SO2水溶液具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
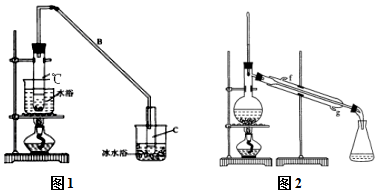 某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯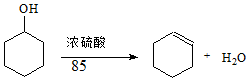
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 | |
| B. | 将一小块钠放入盛有水的烧杯中,钠在水面上游动,同时看到烧杯内的溶液变为红色 | |
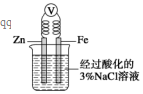
| C. | 如图,一段时间后给烧杯内的溶液中加入氢氧化钠溶液,可看到Fe电极附近有红褐色沉淀生成 | |
| D. | 向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率增大 | B. | 平衡向右移动 | C. | 体系温度升高 | D. | W的质量分数降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
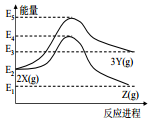
| A. | 由 X→Z 反应的△H<0 | B. | 由 X→Y 反应的△H=E5-E2 | ||
| C. | 增大压强有利于提高 Y 的产率 | D. | 升高温度有利于提高 Z 的产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 上述反应中,每生成2 mol AlN需转移6 mol电子 | |
| C. | AlN中氮元素的化合价为+3 | |
| D. | AlN的摩尔质量为41 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com