
如图所示表示一些元素原子半径规律性的变化示意图。由此图不能得出下列结论的是(不考虑稀有气体元素)( )

A.当电子层数相同时,核电荷数越小,原子半径越大
B.当最外层电子数相同时,质子数越多,原子半径越大
C.r(F-)<r(Cl-)<r(Br-)<r(I-),
r(K+)>r(Na+)>r(Mg2+)>r(Al3+)
D.原子电子层数越多,对应的原子半径越大
科目:高中化学 来源: 题型:
核电荷数小于18的某元素X,其原子核外电子层数为a,最外层 电子数为(2a+1)。下列有关元素X的说法中,不正确的是( )
电子数为(2a+1)。下列有关元素X的说法中,不正确的是( )
A.元素X的原子核内质子数为(2a2-1)
B.元素X的原子半径一定小于钠的原子半径
C.由元素X形成的某些化合物,可能具有杀菌消毒的作用
D.元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对葡萄糖的叙述正确的是( )
A.葡萄糖分子中具有醛基,所以是醛类化合物
B.葡萄糖分子中具有羟基,所以是醇类化合物
C.葡萄糖的结构式可写成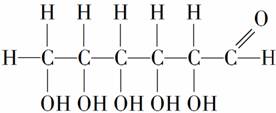
D.葡萄糖是多羟基醛结构,属于糖类化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.燃烧后生成CO2和H2O的有机物必含C、H、O元素
B.符合Cn(H2O)m的有机物必为糖
C.二糖的水解产物不一定全是葡萄糖
D.加热淀粉溶液产生糊化作用
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学课外活动小组探究淀粉水解的条件,进行以下两个实验。
(1)实验用品:0.5 g淀粉、4 mL 20%硫酸、氢氧化钠溶液、银氨溶液、碘水
步骤:在试管1和试管2里各放入0.5 g淀粉,在试管1里加入4 mL 20%硫酸溶液,在试管2里加入4 mL水,都加热3~4 min。用碱液中和试管1里的硫酸溶液,把一部分液体倒入试管3。在试管2、3里都加入碘水,观察有没有蓝色出现。在试管1里加入银氨溶液,稍加热后,观察试管内壁上有无银镜出现。
根据所学知识预测可能的实验现象
实验现象与结论(填入下表):
| 试管 | 加入碘水 | 加入银氨溶液 | 结论 |
| 1 | |||
| 2 | |||
| 3 |
(2)实验用品:0.5 g淀粉、唾液、新制氢氧化铜悬浊液步骤:在试管中加入0.5 g淀粉,加入少许唾液加热,在水解液中加入新制氢氧化铜加热煮沸,观察现象。
现象:__________________________________________________ __________________。
结论:__________________________________________________ __________________。
(3)比较实验(1)(2)可得出的结论:_________________ _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,有关说法正确的是( )
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | b | c | ||||
| 3 | d | e | f | g | h | i |
A.a、b、e、f四种元素的原子半径:e>f >b>a
B.h、i两种元素阴离子的还原性:h>i
C.a、g两种元素氢化物的稳定性:g>a
D.d、e、f三种元素最高价氧化物对应的水化物的碱性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W都是短周期主族元素。其中X原子最外层电子数是内层电子总数的3倍;X、Z同主族,Y、Z同周期,W与X、Y既不同族也不同周期;X、Y、Z三种原子的最外层电子数之和为19。下列说法正确的是( )
A.①Y元素最高价氧化物对应水化物的化学式为:HYO4
B.X、Y、Z形成的简单离子的半径大小为:Yn->Zm->Xm-
C.元素Z、Y分别与元素W形成的化合物的热稳定性为:WmZ<WnY
D.相同条件下,HnY溶液的酸性比HmZ溶液的酸性弱
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应中,硝酸只表现了氧化性的是
A. 3 Cu + 8 HNO3(稀) ======= 3 Cu(NO3)2 + 2 NO↑+ 4 H2O
B. CuO + 2 HNO3(稀) ======= Cu(NO3)2 + H2O
C. C + 4 HNO3(浓) ======= CO2 ↑ + 4 NO2↑ +2 H2O
D. 3 Ag + 4 HNO3(稀) ======= 3 AgNO3 + NO↑ +2 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化钠是日常生活中人们常用的调味品。下列性质可以证明氯化钠中一定存在离子键的是( )
A.具有较高的熔点 B.熔融状态下能导电
C.水溶液能导电 D.常温下能溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com