
| A. | 1mol | B. | 3mol | C. | 4mol | D. | 6mol |
分析 油脂与NaOH反应的物质的量之比为1:3,n(NaOH)=$\frac{1.8g}{40g/mol}$=0.045mol,则10 g油脂的物质的量为n(油脂)=$\frac{1}{3}$n(NaOH)=0.045mol×$\frac{1}{3}$=0.015 mol,则油脂的摩尔质量=$\frac{10g}{0.015mol}$,n(H2)=$\frac{12g}{2g/mol}$=6mol,1000.0g油脂的物质的量=$\frac{\frac{1000g}{10g}}{0.015mol}$=1.5mol,根据油脂的物质的量与氢气的物质的量确定油脂中含有的碳碳双键个数.
解答 解:油脂与NaOH反应的物质的量之比为1:3,n(NaOH)=$\frac{1.8g}{40g/mol}$=0.045mol,则10 g油脂的物质的量为n(油脂)=$\frac{1}{3}$n(NaOH)=0.045mol×$\frac{1}{3}$=0.015 mol,则油脂的摩尔质量=$\frac{10g}{0.015mol}$,n(H2)=$\frac{12g}{2g/mol}$=6mol,1000.0g油脂的物质的量=$\frac{\frac{1000g}{10g}}{0.015mol}$=1.5mol,油脂和氢气的物质的量之比=1.5mol:6mol=1:4,一个碳碳双键加成需要1分子氢气,所以一个油脂分子中含有4个碳碳双键,则1mol该油脂中平均含碳碳双键4mol,
故选C.
点评 本题考查了有机物中化学键的计算,根据反应中各个物理量之间的关系式来分析解答,灵活运用基本公式,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
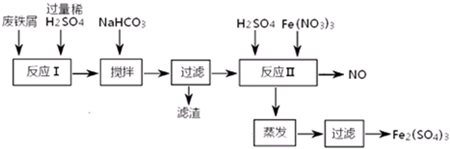
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 氯气和氢氧化钠溶液或石灰乳反应得到的含氯化合物都具有漂白性 | |
| C. | 光导纤维遇强酸会“断路” | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①③④ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com