
【题目】填空题
(1)已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去): 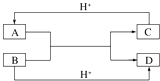
①如果A、B、C、D均是10电子的粒子,请写出:A电子式:;D的结构式: .
②如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:A与B在溶液中反应的离子方程式为 . 根据上述离子方程式,可以判断C与B结合质子的能力大小是 . (用化学式或离子符号表示).
(2)另一10电子物质,相同条件下对H2的相对密度为8,常温常压下,3.2g该物质与足量氧气充分燃烧后放出akJ热量,(a>0).写出该物质燃烧热的热化学方程式: .
将3.2g该物质燃烧后的产物通入100mL3molL﹣1的NaOH溶液中,充分反应后所得的溶液中离子浓度大小关系为: .
【答案】
(1)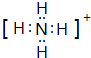 ;H﹣O﹣H;HS﹣+OH﹣═S2﹣+H2O;OH﹣>S2﹣
;H﹣O﹣H;HS﹣+OH﹣═S2﹣+H2O;OH﹣>S2﹣
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣5akJ?mol﹣1;Na+>HCO3﹣>CO32﹣>OH﹣>H+
【解析】解:(1.)①10电子微粒A、B反应得到两种10电子微粒,应是铵根离子与氢氧根离子反应得到氨气与水,而C、B都能与氢离子反应,可推知A为NH4+ , B为OH﹣ , C为NH3 , D为H2O,NH4+的电子式为 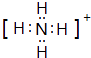 ,H2O结构式为H﹣O﹣H,
,H2O结构式为H﹣O﹣H,
所以答案是: 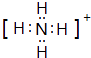 ;H﹣O﹣H;
;H﹣O﹣H;
②如果A、C均是18电子的粒子,B、D是10电子粒子,结合转化关系,可推断:A为H2S,B为OH﹣ , C为HS﹣或S2﹣ , D为H2O,A与B在溶液中反应的离子方程式为:HS﹣+OH﹣═S2﹣+H2O,根据离子方程式,可以判断结合质子的能力大小是OH﹣>S2﹣ , 所以答案是:HS﹣+OH﹣═S2﹣+H2O;OH﹣>S2﹣;
(2.)另一10电子物质,相同条件下对H2的相对密度为8,则该物质相对分子质量为16,则该物质为CH4 , 1mol甲烷燃烧放出的热量为akJ× ![]() =5a kJ,反应热书写热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣5akJmol﹣1;
=5a kJ,反应热书写热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣5akJmol﹣1;
3.2g甲烷物质的量为 ![]() =0.2mol,则燃烧生成二氧化碳为0.2mol,NaOH物质的量为0.1L×3mol/L=0.3mol,由于1:2<n(CO2):n(NaOH)=2:3<1:1,而生成NaHCO3、Na2CO32 , 设二者物质的量分别为xmol、ymol,根据钠离子守恒、碳原子守恒可得:
=0.2mol,则燃烧生成二氧化碳为0.2mol,NaOH物质的量为0.1L×3mol/L=0.3mol,由于1:2<n(CO2):n(NaOH)=2:3<1:1,而生成NaHCO3、Na2CO32 , 设二者物质的量分别为xmol、ymol,根据钠离子守恒、碳原子守恒可得: ![]() ,解得x=y=0.1,结合溶液中HCO3﹣、CO32﹣水解呈碱性,且碳酸根离子水解程度大于碳酸氢根的,故溶液中离子浓度大小为:Na+>HCO3﹣>CO32﹣>OH﹣>H+ ,
,解得x=y=0.1,结合溶液中HCO3﹣、CO32﹣水解呈碱性,且碳酸根离子水解程度大于碳酸氢根的,故溶液中离子浓度大小为:Na+>HCO3﹣>CO32﹣>OH﹣>H+ ,
所以答案是:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣5akJmol﹣1; Na+>HCO3﹣>CO32﹣>OH﹣>H+ .


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:
【题目】硫代硫醉钠又名“大苏打”,溶液具有弱碱性和较强的还原性,是棉织物漂白后的脱氯剂,定量分析中的还原剂.硫代硫酸钠(Na2S203)可由亚硫酸钠和硫粉通过化合反应制得,装置如图I所示.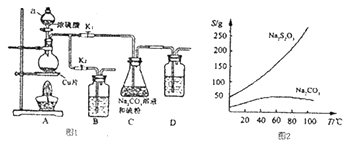
已知:Na2S2O3在酸性溶液中不能稳定存在,有关物质的溶解度曲线如图2所示.
(1)Na2S2O35H2O的制备:
步骤1:如图连接好装置后(未装药品),检查A、C装且气密性的操作是_ .
步骤2:加人药品,打开K1、关闭K2、加热.装置B、D中的药品可选用下列物质中的(填编号).
A.NaOH溶液 B.浓H2SO4C.酸性KMnO4溶液 D.饱和NaHCO3溶液
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的最逐渐减少.
步骤4:过滤C中的混合液,将滤液经过加热浓缩,趁热过滤,再将滤液过滤、洗涤、烘干,得到产品.
(2)Na2S2O3性质的检验:向足量的新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,检查反应后溶液中含有硫酸根,写出该反应的化学方程式 .
(3)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加人足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解.此时Cr42﹣全部转化为Cr2O72﹣;再加过量KI溶液,充分反应后,加入淀粉溶液作指示剂,用0.010molL﹣1的Na2S2O3溶液进行滴定,反应完全时,消耗Na2S2O3溶液18.00mL.部分反应的离子方程式为:Cr2O72﹣+6I﹣+14H+═2Cr3++3I2+7H2O.I2+2S2O32﹣═S4O62﹣+2I﹣ , 则该废水中Ba2+的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘元素,某学习小组设计如下实验流程提取海带中的碘,请回答下列问题:
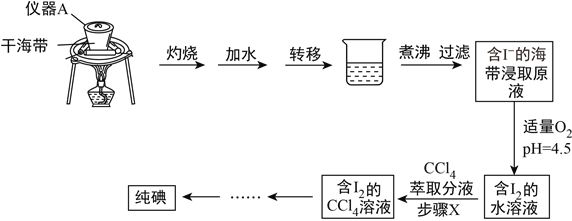
(1)仪器A的名称为__________________,实验室取用仪器A必须使用_________。
(2)煮沸的作用是______________________。
(3)步骤X中,使用了分液漏斗。分液漏斗使用前,须进行的操作是__________;萃取后,分液漏斗内观察到的现象是___________;分液时,为了保证液体顺利留下,应首先_________。
(4)向海带浸取原液中通入适量O2,并控制溶液pH为4.5,此时发生反应的离子反应方程式为:__________________________________________。
(5)某同学欲采用蒸馏含I2的CCl4溶液得到纯碘,此方案不合理,理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用托盘天平称量镁粉25.2g(1g以下用游码),他把镁粉放在右盘,当天平平衡时,所称取的镁粉的实际质量是
A. 25.2g B. 24.8g C. 24.2g D. 26.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,PH=9的碳酸钠溶液中由水电离出的c(OH﹣)=1×10﹣9molL﹣1
B.饱和氯水中:c(Cl﹣)=c(ClO﹣)+c(HClO)
C.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
D.中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科技的发展,阿伏加德罗常数的测定手段越来越多,测定精确度也越来越高,现有一种简单可行的测定方法,具体步骤为:
(1)将固体NaCl研细、干燥后,准确称取mg NaCl固体并转移到定容仪器A中。
(2)用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为Vcm3。请回答下列问题:
①步骤(1)中A仪器最好用__________(填序号)
A.量筒 B.烧杯 C.容量瓶 D.试管
②能否用水代替苯_______,理由是______________________。
③NaCl晶体中,Na+和Cl-是按一定方式有规则均匀排列的,可以看作一系列立方体在空间的延伸。已知立方体的边长为acm,它拥有b个钠离子和b个氯离子,用上述测定方法测得的阿伏加德罗常数NA的表达式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向密闭恒容容器中加入1.0mol/L X,发生反应:2X(g)Y(g)+Z(g),△H<0,反应到8min时达到平衡;在14min时改变的温度,16min时建立新平衡.X的物质的量浓度变化如图所示.下列有关说法正确的是( ) 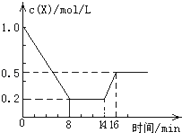
A.0~8min用Y表示的该反应的速度为0.1mol/Lmin
B.8min时达到平衡,该反应的平衡常数为 K=0.5
C.14min时,改变的反应条件是降低了体系的温度
D.16min时的正反应速率,比8min时的正反应速率大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前从海水中提取的溴占世界溴年产量的三分之一左右,常用的方法之一是用氧化剂把溴离子氧化成单质,再通入热空气将溴蒸气吹出,这一反应中常用的氧化剂是( )。
A. Cl2B. Br2C. H2OD. H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA﹣ , Ⅲ代表A2﹣)所示.根据图示判断,下列说法正确的是( ) 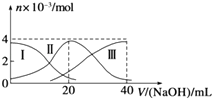
A.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA﹣)>c(A2﹣)>c(H+)>c(OH﹣)
B.等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水小
C.NaHA溶液中:c(OH﹣)+c(A2﹣)=c(H+)+c(H2A)
D.向上述加入20mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com