
| A. | 铵态氮肥不能与草木灰混合使用 | |
| B. | 大力推进小火力发电站的兴建,以缓解地方用电困难 | |
| C. | 医学上,常使用BaSO4做内服造影剂 | |
| D. | 为防止电池中重金属等污染环境和水体,应积极开发废旧电池的综合技术 |
分析 A.依据盐类水解的性质解答;
B.小火力发电站容易造成资源浪费,环境污染;
C.硫酸钡不溶液盐酸;
D.废旧电池含有重金属汞、镉等.
解答 解:A.草木灰中的碳酸根离子水解显碱性,铵态氮肥中铵根离子水解显酸性,二者相互促进,导致肥效降低,所以不能混合使用,故A正确;
B.小火力发电站容易造成资源浪费,环境污染,应减少小火力发电站的兴建,故B错误;
C.硫酸钡不溶液盐酸,可以做内服造影剂,故C正确;
D.废旧电池含有重金属汞、镉等,为防止环境污染,应积极开发废旧电池的综合技术,故D正确;
故选:B.
点评 本题考查了化学与社会生活,主要涉及环境污染与治理,明确盐类水解的应用,硫酸钡的性质是解题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 碘单质受热升华:紫色蒸气 | B. | 硫磺在氧气中燃烧:蓝紫色的火焰 | ||
| C. | 铁丝在氯气中燃烧:棕褐色的烟 | D. | 氢气在氯气中燃烧:淡蓝色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们形成的离子化合物化学式为AB2 | |
| B. | 原子序数:A一定大于B | |
| C. | A和B形成的离子电子层结构一定相同 | |
| D. | A一定是金属,B一定是非金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
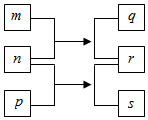 W、X、Y、Z是原子序数依次增大的短周期元素.m、n、p是由这些元素组成的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q的水溶液呈碱性,0.01mol•L-1s溶液的pH为12,q、s的焰色反应均呈黄色.上述物质的转化关系如图所示.下列说法正确的是( )
W、X、Y、Z是原子序数依次增大的短周期元素.m、n、p是由这些元素组成的二元化合物,r是元素Y的常见单质,能使带火星的木条复燃,q的水溶液呈碱性,0.01mol•L-1s溶液的pH为12,q、s的焰色反应均呈黄色.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:W<X<Y<Z | |
| B. | Y的氢化物的沸点比Z的氢化物的沸点高 | |
| C. | 通常状况下,X的氢化物可能呈气态、液态或固态 | |
| D. | 由W、X、Y、Z四种元素只能组成一种化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a=1.0时,反应的离子方程式为:Ba2++2OH-+CO2═BaCO3↓+H2O | |
| B. | 当a=1.5时,反应的离子方程式为:2Ba2++6OH-+3CO2═2BaCO3↓+CO32-+3H2O | |
| C. | 当a=2.5时,反应的离子方程式为:OH-+CO2═HCO3- | |
| D. | 当a=1.75时,溶液中HCO3与CO32-的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
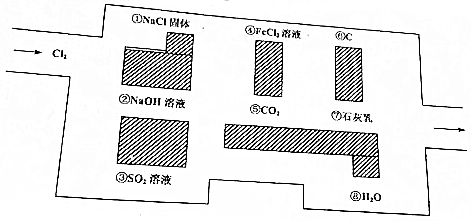
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ω=$\frac{w}{w+V}$×100% | B. | S=$\frac{w}{V}$×100g | ||
| C. | c=$\frac{1000w}{MV}$mol•L-1 | D. | c=$\frac{1000aw}{M(w+V)}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
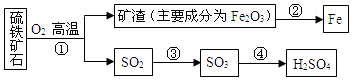
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 水的离子积常数Kw与温度无关 | |
| C. | 溶液中c(Ag+)•c(Cl-)大于Ksp时,将产生AgCl | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=xmol/L,c(B-)=ymol/L,则Ksp值为xy |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com