
| A.④⑤③ | B.⑥①⑤③ | C.⑥⑤①② | D.⑦① |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
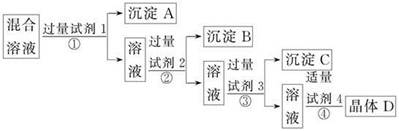
| A.氯化钡溶液、硝酸银溶液、碳酸钠溶液、硝酸溶液 |
| B.硝酸银溶液、氯化钡溶液、碳酸钠溶液、硝酸溶液 |
| C.氯化钡溶液、硝酸银溶液、硝酸溶液、碳酸钠溶液 |
| D.硝酸银溶液、碳酸钠溶液、氯化钡溶液、硝酸溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
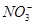 、
、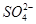 、Cl-、I-、
、Cl-、I-、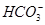 ,取该溶液进行实验:
,取该溶液进行实验:| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊试液 | 溶液变红 |
| (2)取少量该溶液加热,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.试管中盛酚酞溶液,验证氨气的水溶液呈碱性 |
| B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性 |
| C.试管中盛稀氢氧化钠溶液,验证CO2与NaOH反应的产物 |
| D.试管中盛淀粉KI溶液,验证氯气的氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
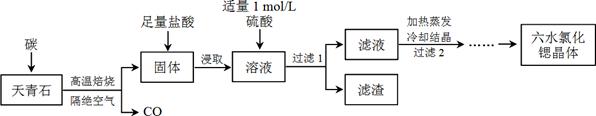
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用酒精萃取碘水中的碘 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,并过滤 |
| ② | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
| ③ | CH4 | C2H4 | 通过盛有酸性高锰酸钾溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 溶解、过滤、蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 )=2.50×10-4 mol·L-1,则Ca2+_ _____(填“是”或“否”)沉淀完全。[已知c(Ca2+)≤10-5 mol·L-1可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
)=2.50×10-4 mol·L-1,则Ca2+_ _____(填“是”或“否”)沉淀完全。[已知c(Ca2+)≤10-5 mol·L-1可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]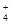 ) c(NO
) c(NO ) (填 > 、< 或 = ),(NH4)2CO3溶液中离子浓度由大到小的顺序为 。
) (填 > 、< 或 = ),(NH4)2CO3溶液中离子浓度由大到小的顺序为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁粉中混有铝粉:加入过量烧碱溶液充分反应后过滤 |
| B.FeCl2溶液中混有FeCl3:加入过量铁粉充分反应后过滤 |
| C.Na2CO3固体中混有少量NaHCO3:加入过量NaOH溶液,反应后加热蒸干 |
| D.氯气中混有少量氯化氢气体:将混合气体通过盛饱和食盐水的洗气瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com