
设NA是阿伏加德罗常数的数值,下列说法正确的是( )
|
| A. | 1molAl3+离子含有的核外电子数为10NA |
|
| B. | 1molCl2与足量的铁反应,转移的电子数为3NA |
|
| C. | 10LpH=1的硫酸溶液中含有的H+离子数为2NA |
|
| D. | 10LpH=13的NaOH溶液中含有的OH﹣离子数为NA |
| 阿伏加德罗常数. | |
| 专题: | 阿伏加德罗常数和阿伏加德罗定律. |
| 分析: | A、铝离子核外有10个电子,1mol铝离子含有10mol电子; B、根据电荷守恒,1mol氯气完全反应转移2mol电子; C、PH=1,溶液中氢离子浓度是0.1mol/L,10L溶液中含有1mol氢离子; D、PH=13,溶液中氢氧根离子的浓度是0.1mol/L,10L溶液中含有1mol氢氧根离子. |
| 解答: | 解:A、由于铝离子核外有10个电子,1mol铝离子含有10mol电子,核外电子数为10NA,故A正确; B、1mol氯气完全反应转移2mol电子,转移的电子数为2NA,故B错误; C、由于PH=1,硫酸溶液中氢离子浓度是0.1mol/L,10L溶液中含有1mol氢离子,含有的H+离子数为1NA,故C错误; D、由于PH=13,氢氧化钠溶液中氢氧根离子的浓度是0.1mol/L,10L溶液中含有1mol氢氧根离子,含有的OH﹣离子数为NA,故D正确; 故选AD. |
| 点评: | 本题考查了阿伏伽德罗常数,注重了基础知识的考查,本题难度不大. |


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
将11.5 g钠、9 g铝、28 g铁分别投入200 mL 1 mol·L-1的盐酸中,结果正确的是( )
A.钠与盐酸反应最剧烈,产生的气体最多
B.铝与盐酸反应的速率仅次于钠,但产生的气体最多
C.铁与盐酸反应产生的气体比钠多
D.反应结束时产生的气体一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
经测定,H2O2为二元弱酸,其酸性比碳酸弱,它在碱性溶液中极不稳定,易分解生成H2O和O2。若向Na2O2中通入干燥的CO2气体,Na2O2与CO2并不起反应。
(1)写出H2O2在水溶液中的电离方程式
(2)用化学方程式表示Na2O2和潮湿的CO2气体反应的过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
在如图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹夹在被Na2SO4溶液浸湿的滤纸条上。滤纸条的中部滴有KMnO4液滴;电源有a、b两极。在A、B 中充满KOH溶液后倒立于KOH溶液的水槽中,切断K1,闭合K2、K3,通直流电。
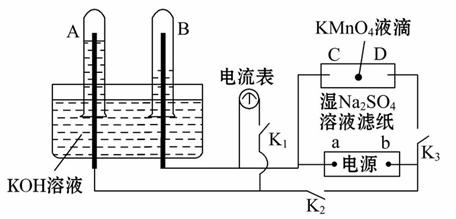
(1)写出B中电极反应式____________________________________________ ___。
___。
(2)在湿的硫酸钠溶液滤纸条中部的高锰酸钾液滴处发生的现象是__________。
(3)电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针__________(填“是”或“否”)移动,其理由是_____________。
(4)在298 K时,若2 g B气体和0.5 mol的A气体完全反应,生成物为液态,放出285.8 kJ热量,写出此反应的热化学方程式:______________________
__________ ________________________________________________________。
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在碱性溶液中能大量共存且为无色透明的溶液是( )
|
| A. | K+、Cl﹣、MnO4﹣、SO42﹣ | B. | Na+、Cu2+、NO3﹣、CO32﹣ |
|
| C. | Na+、NO3﹣、SO42﹣、HCO3﹣ | D. | Na+、SO42﹣、Cl﹣、NO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
能在溶液中大量共存的一组离子是( )
|
| A. | NH4+、Ag+、PO43﹣、Cl﹣ | B. | Fe3+、H+、I﹣、HCO3﹣ |
|
| C. | K+、Na+、NO3﹣、MnO4﹣ | D. | Al3+、Mg2+、SO42﹣、CO32﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
请回答下列问题:
(1)T的原子结构示意图为 .
(2)元素的非金属性为(原子的得电子能力):Q W(填“强于”或“弱于”).
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为 .
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 .
(5)R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 .
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ.又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H= (注:题中所涉单质均为最稳定单质).

查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应:Co2O3 + 6HCl(浓) == 2CoCl2 + Cl2↑+ 3H2O (I)

(1)反应(I)中的氧化剂是
(2)根据反应(I)计算,若生成标准状况下33.6L氯气时,电子转移数目是
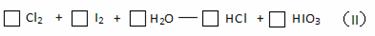 (3)将反应(II)配平
(3)将反应(II)配平
(4)反应(II) 中 发生氧化反应(5)HCl 、I2 、CoCl2三种物质的还原性由强到弱的顺序是
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验对应的结论不正确的是
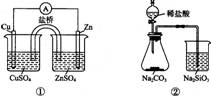
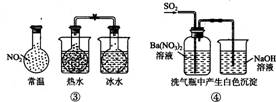
A.①能组成Zn-Cu原电池 B.②能证明非金属性Cl>C>Si
C.③能说明2NO2 N2O4 △H<0 D.④中自色沉淀为BaSO4
N2O4 △H<0 D.④中自色沉淀为BaSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com