
| A. | 1,4-丁二醇的键线式: | B. | CH3+的电子式: | ||
| C. | 麦芽糖的实验式:CH2O | D. | 聚甲醛的结构简式: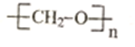 |
分析 A.键线式:拐点和端点表示碳原子,碳原子,H不必标出,杂原子(非碳、氢原子)不得省略,并且其上连有的氢也一般不省略;
B.CH3+是缺电子的碳正离子,不是呈电中性的原子团;
C.实验式是用元素符号表示化合物分子中各元素的原子个数比的最简关系式;
D.甲醛含有双键可以发生加聚反应,生成聚甲醛.
解答 解:A.1,4-丁二醇的结构简式HOCH2CH2CH2CH2OH,键线式碳原子、氢原子不必标出,1,4-丁二醇的键线式为: ,故A错误
,故A错误
B.因碳原子最外层4个电子,则CH3+是缺电子的碳正离子,可看作是甲基失去一个电子后的产物,甲基的电子式为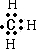 ,则CH3+的电子式为
,则CH3+的电子式为 ,故B错误;
,故B错误;
C.麦芽糖为二糖,分子式为C12H22O11,实验式为:C12H22O11,故C错误;
D.甲醛分子的结构式: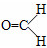 ,含有双键可以发生加聚反应,生成聚甲醛,聚甲醛结构简式为
,含有双键可以发生加聚反应,生成聚甲醛,聚甲醛结构简式为 ,故D正确;
,故D正确;
故选D.
点评 本题考查了键线式、电子式、实验式、结构简式等表示方法的判断,题目难度中等,注意掌握电子式、聚甲醛的结构简式等化学用语的概念及表示方法.


科目:高中化学 来源: 题型:解答题

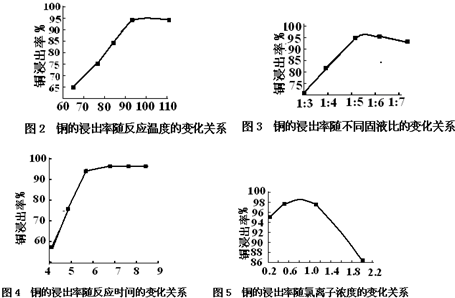
| 反应温度/℃ | 固液比 | c(Cl-)/mol•L-1 | 反应时间/h | |
| A | 95 | 1:5.5 | 0.8 | 6 |
| B | 100 | 1:5.5 | 0.7 | 7 |
| C | 110 | 1:6 | 0.9 | 8 |
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 40.01 |
| 2 | 25.00mL | 0.70 | 40.71 |
| 3 | 25.00mL | 0.20 | 39.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
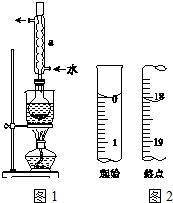 Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离出的C(H+)=10-13mol/L的溶液中K+、NO3-、Br-、Cl- | |
| B. | 含有大量NO3-的水溶液:I-、Fe3+、H+、Na+ | |
| C. | 弱碱性溶液中HCO3-、NH4+、C2H5O-、MnO4- | |
| D. | 无色透明溶液中:Ba2+、S2-、Cu2+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y、Z元素最高价氧化物对应的水化物酸性较强的为H2ZO4 | |
| B. | 离子半径由大到小的顺序为:W>Z>Y | |
| C. | X、Z两种元素的气态氢化物中,X的气态氢化物较稳定,因为X的氢化物分子间有氢键 | |
| D. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiH4、PH3、H2S、HCl | B. | HF、HCl、HBr、HI | ||
| C. | PH3、H2S、HCl、HF | D. | NH3、PH3、AsH3、HF |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com