
| 1 |
| 2 |
| 500mL |
| 20mL |
| 7.95g |
| 106g/mol |
| 2g |
| 500g |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
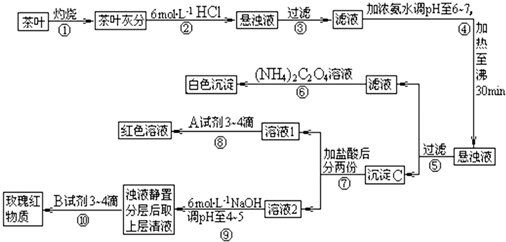
【查阅部分资料】草酸铵〔(NH4)2C2O4〕属于弱电解质。草酸钙(CaC2O4)难溶于水。Ca2+、Al3+、Fe3+完全沉淀的pH:Ca(OH)2:pH≥13;Al(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1。

试根据上述过程及信息填空:
(1)步骤②加盐酸的作用是____________________________________________________。
(2)写出检验Ca2+的离子方程式________________________________________________。
(3)写出沉淀C所含主要物质的化学式____________。
(4)写出步骤⑧用A试剂生成红色溶液的离子方程式______________________________。
(5)步骤⑨的作用是_________________,猜测步骤⑩的目的是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com