
用标准的NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是
A.盛装标准液的滴定管未用标准液润洗
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定前无气泡,滴定到终点时,发现尖嘴处有气泡
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届江苏省宿迁市三校高三9月学情调研化学试卷(解析版) 题型:填空题
(12分)铁在地壳中的含量约占 5 %左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是 Fe2O3)等。
(1)红热的铁能跟水蒸气反应,一种产物与磁铁矿的主要成分相同,另一种产物是可燃性气体,则其反应的化学方程式为 。该可燃气体在酸性条件下,可制成燃料电池,写出该气体发生的电极反应式 。
(2)在常温下,铁跟水不起反应。但在潮湿的空气中,铁很容易生锈(铁锈的主要成分是 Fe2O3)而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。铁生锈的化学原理如下,请你用离子方程式和化学方程式补充完整。
①原电池反应:
负极:2Fe-4e-=2Fe2+、正极: ;
②氢氧化物的形成: Fe2 + + 2OH-= Fe(OH)2↓ 。
③氢氧化物的分【解析】
2Fe(OH)3 =Fe2O3+3H2O。
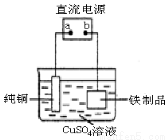
(3)为了防止铁生锈,可在铁制品表面镀上一层铜(如图装置),a为 (填“正极”或“负极”),铁制品表面发生的电极反应式 为 。
查看答案和解析>>
科目:高中化学 来源:2016届河南省濮阳市心高三上第一次市统摸底化学试卷(解析版) 题型:选择题
下列表示对应反应的离子方程式正确的是
A.向稀 HNO3 中滴加 Na2SO3 溶液:SO32-+2H+=== SO2↑+H2O
B.双氧水中加入稀硫酸和KI溶液: H2O2+ 2I-+2H+=I2+ 2H2O
C.向 Al2(SO4)3 溶液中加入过量 NH3•H2O:Al3++4NH3•H2O === AlO2-+ 4NH4+ + 2H2O
D.醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市高三第一学期第一次月考化学试卷(解析版) 题型:选择题
发射“天宫一号”的长三丙火箭由三个子级构成。其一级发动机内燃烧的化学方程式为:
C2H8N2(l)+2N2O4(l)―→3N2(g)+2CO2(g)+4H2O(g)+5986KJ,该反应中
A.C2H8N2发生还原反应
B.C2H8N2是氧化剂
C.N2O4发生氧化反应
D.N2O4是氧化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省白城市高一上第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是
A.标准状况下,48gO3含有的氧原子数为3NA
B.1molOH-离子中含电子数目为10NA
C.0.5L 0.2mol·L-1的NaCl溶液中含有的Na+数是0.1NA
D.常温常压下,33.6LCO中含有的原子数是3NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二上第一次月考化学试卷(解析版) 题型:选择题
在100 mL 0.1 mol·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是
A.加热
B.加入100 mL 0.1 mol·L-1的醋酸溶液
C.加入少量的0.5 mol·L-1的硫酸
D.加入少量的1 mol·L-1的NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是
①向饱和碳酸钠溶液中通入过量的CO2;
②向NaAlO2溶液中逐滴加入过量的稀盐酸;
③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液;
④向硅酸钠溶液中逐滴加入过量的盐酸
A.①② B.①③ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二开学考试化学试卷(解析版) 题型:填空题
(10分)(1)在一个固定体积为2升的密闭容器中,充入2molA和1molB,发生如下反应:2A(g)+B(g) 3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
①2分钟内用B表示的平均反应速度为 ;
②若容器温度升高,平衡时混合气体的平均摩尔质量减小,则正反应为 (填“吸热”或“放热”)反应。
(2)一定温度下,在一定容积的密闭容器中发生如下可逆反应:
2A(g)+B(g) 2C(g)
2C(g)
在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。

试回答下列问题:
①A点时,反应的v(正)v(逆)(填“>”、“<”或“=”);
②此反应的逆反应为 热反应(填“放”或“吸”);
③A、B两点的正反应速率:v(A)v(B)(填“>”、“<” 或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com