
| A. |  | B. |  | C. |  | D. | 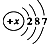 |
分析 粒子结构示意图中,当质子数=核外电子数时为原子;当质子数>核外电子数时为阳离子;当质子数<核外电子数时为阴离子,据此进行分析解答.
解答 解:A. 的最外层为3个电子,核外电子总数为13,表示的是铝原子,故A错误;
的最外层为3个电子,核外电子总数为13,表示的是铝原子,故A错误;
B.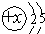 的最外层为5个电子,核外电子总数为7,表示的是氮原子,故B错误;
的最外层为5个电子,核外电子总数为7,表示的是氮原子,故B错误;
C.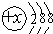 可以为Ar原子,也可以为阴离子,如氯离子、硫离子等,还可以表示阳离子,如钾离子、钙离子等,故C正确;
可以为Ar原子,也可以为阴离子,如氯离子、硫离子等,还可以表示阳离子,如钾离子、钙离子等,故C正确;
D.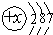 最外层7个电子,核外电子总数为17,表示的为氯原子,故D错误;
最外层7个电子,核外电子总数为17,表示的为氯原子,故D错误;
故选C.
点评 本题考查了粒子结构示意图的表示方法判断,题目难度不大,注意掌握粒子结构示意图的表示方法,明确原子结构示意图、离子结构示意图的区别.


科目:高中化学 来源: 题型:选择题
| A. | 2molA 1molB | B. | 2molA 2molB | C. | 2molC 4molD | D. | 2molC 2molD |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)═c(SO42-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 0.1 mol/L Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| C. | 物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═2c(HCO3-)+2c(H2CO3)+2c(CO32-) | |
| D. | pH=1的NaHSO4溶液:c(H+)═2c(SO42-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 a、b、c、d、e、f是原子序数依次增大的6种短周期元素,a、d同主族,a是原子半径最小的元素,b的最高正化合价与最低负化合价的代数和为零,a与c、d与c均可形成原子个数之比为2:1和1:1的化合物,d、e的最外层电子数之和等于b的最外层电子数,f是同周期中得电子能力最强的元素.
a、b、c、d、e、f是原子序数依次增大的6种短周期元素,a、d同主族,a是原子半径最小的元素,b的最高正化合价与最低负化合价的代数和为零,a与c、d与c均可形成原子个数之比为2:1和1:1的化合物,d、e的最外层电子数之和等于b的最外层电子数,f是同周期中得电子能力最强的元素. .a、c、d三种元素形成的化合物中存在的化学键类型是离子键、共价键.
.a、c、d三种元素形成的化合物中存在的化学键类型是离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、NH4+、SCN-、Cl- | B. | Fe3+、H+、NO3-、SO42- | ||
| C. | K+、H+、NO3-、AlO2- | D. | Na+、NH4+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:6 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com