
| A. | 1L 0.1mol•L-1的氨水含有0.1 NA个OH- | |
| B. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| C. | 80℃时,1L pH=1的硫酸溶液中,含有0.2NA个H+ | |
| D. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA |
分析 A.NH3•H2O是弱电解质,存在电离平衡;
B.标准状况下气体摩尔体积为22.4L/mol,常温常压下的33.6L氯气的物质的量小于1.5mol;
C.1L pH=1的硫酸溶液中,n(H+)=cV;
D.阴极析出32g铜的物质的量为0.5mol,根据电极反应和电子守恒计算;
解答 解:A.NH3•H2O是弱电解质,1L 0.1mol•L-1的氨水含有的OH-小于0.1NA,故A错误;
B.标准状况下气体摩尔体积为22.4L/mol,常温常压下的33.6L氯气的物质的量小于1.5mol,2Al+3Cl2=2AlCl3,故27g铝不能完全反应,转移的电子数小于3NA,故B错误;
C.1L pH=1的硫酸溶液中,c(H+)=0.1mol•L-1,n(H+)=0.1mol,含有0.1NA个H+,故C错误;
D.阴极析出32g铜的物质的量为0.5mol,电极反应为:Cu2++2e-=Cu,根据电子守恒,转移电子数为NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,熟练掌握公式的使用和物质的结构是解题关键.


科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 过滤时,引流的玻璃棒下端触在三层滤纸处 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 用pH试纸测溶液的酸性时,应先将试纸用蒸馏水润湿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 页岩气是一种新型的能源,主要成分是甲烷和少量液态烃及CO2,使用页岩气可以有效地降低碳排放量,减少温室效应 | |
| B. | 针对H7N9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、活性银离子、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学核心 | |
| C. | 李比希基团理论、逆合成分析理论、范特霍夫对有机化合物结构的三维认识都为有机化学的发展作出贡献 | |
| D. | 石油加工工艺除常见的裂化外,还有催化重整和加氢裂化等工艺,它们都是为了提高汽油等轻质油品质;催化重整还是获得芳香烃的主要途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
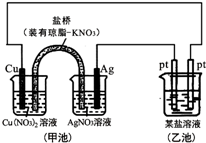
| A. | 图中甲池为原电池装置,电子从铜电极通过溶液和盐桥流向Ag电极 | |
| B. | 实验过程中,甲池左侧烧杯中NO3-的浓度不变 | |
| C. | 若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量不变 | |
| D. | 若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液不可能是AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、HBr、HI的熔沸点依次升高 | |
| B. | 乙醇分子与水分子之间只存在范德华力 | |
| C. | 甲醇的熔点、沸点大于甲烷是由于甲醇分子之间存在氢键 | |
| D. | 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过红外光谱分析可以区分乙醇和乙酸 | |
| B. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 | |
| C. | 光催化还原水制氢比电解水制氢更节能环保、更经济 | |
| D. | 石油的裂解、煤的干馏、蛋白质的盐析和淀粉的水解都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 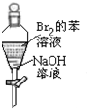 充分振荡后静置,上层溶液颜色保持不变 | |
| B. | 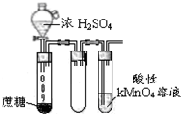 酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 | |
| C. | 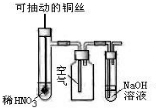 微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 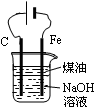 制备Fe(OH)2并能较长时间观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
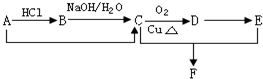 已知某烃A的产量是衡量一个国家石油化工水平的标志,能发生下列转化关系(部分反应物或生成物及反应条件已略去):
已知某烃A的产量是衡量一个国家石油化工水平的标志,能发生下列转化关系(部分反应物或生成物及反应条件已略去):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com