

 H2TiO3+2H+,当加入热水稀释、升温后,平衡正向移动,生成H2TiO3。
H2TiO3+2H+,当加入热水稀释、升温后,平衡正向移动,生成H2TiO3。 H2TiO3+2H+,水解反应是吸热反应。当加入热水升高温度后,促进盐的水解,水解平衡正向移动,会生成更多的H2TiO3,从而促使物质的转化。(5)①在原来的溶液中含有Fe3+,以以KSCN溶液为指示剂,此时溶液是红色,其中存在平衡:Fe3++3SCN-
H2TiO3+2H+,水解反应是吸热反应。当加入热水升高温度后,促进盐的水解,水解平衡正向移动,会生成更多的H2TiO3,从而促使物质的转化。(5)①在原来的溶液中含有Fe3+,以以KSCN溶液为指示剂,此时溶液是红色,其中存在平衡:Fe3++3SCN- Fe(SCN)3.随着铝粉的不断加入,c(Fe3+)不断降低,平衡逆向移动,红色逐渐变浅,当滴入最后一滴NH4Fe(SO4)2溶液时,溶液变为血红色且半分钟内不褪色,则说明达到终点;②根据电子转移数目相等可得关系式:3TiO2+~Al~3Fe3+.n(Fe3+)="0.1mol/L×0.03L×5=0.015mol." n(TiO2+)=" 0.015mol," 所以待测钛液中TiOSO4的物质的量浓度是c(TiO2+)= 0.015mol÷0.01L=1.50mol/L.
Fe(SCN)3.随着铝粉的不断加入,c(Fe3+)不断降低,平衡逆向移动,红色逐渐变浅,当滴入最后一滴NH4Fe(SO4)2溶液时,溶液变为血红色且半分钟内不褪色,则说明达到终点;②根据电子转移数目相等可得关系式:3TiO2+~Al~3Fe3+.n(Fe3+)="0.1mol/L×0.03L×5=0.015mol." n(TiO2+)=" 0.015mol," 所以待测钛液中TiOSO4的物质的量浓度是c(TiO2+)= 0.015mol÷0.01L=1.50mol/L.

科目:高中化学 来源:不详 题型:单选题
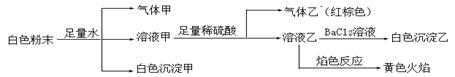
| A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和HCO3- |
| B.气体乙一定是NO和NO2的混合气体 |
| C.白色沉淀乙是BaSO4,所以原混合物一定含有SO42- |
| D.白色粉末中一定含有Na+ 、Al3+ 、NO2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大 |
| B.1 mol·L-1的NH4Cl溶液中含有NH4+的数目一定小于NA |
| C.用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-=2Fe(OH)3↓+3H2↑ |
| D.将带有相反电荷的胶体混合,一定会出现胶体聚沉现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c (Na+)=c(CH3COO-)+c(CH3COOH) |
| B.c(H+)=c(CH3COO-)+c(OH一) |
| C.c (Na+) > c (CH3COO-)>c(OH-)>c(H+) |
| D.c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
 ) (填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH
) (填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH )。
)。 )-c(NH
)-c(NH )-3c(Al3+)= mol·L-1。
)-3c(Al3+)= mol·L-1。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾、氯化铁晶体常用于净水或消毒 |
| B.实验室通常使用热的纯碱溶液去除油污 |
| C.实验室配制FeCl3溶液时加入少量稀盐酸 |
| D.实验室制氢气时加入CuSO4可加快反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com