
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是
A. 2gD2O和H2l8O混合物中所含中子数为NA
B. 1L0.1mol·L-1 NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
C. 常温常压下,0.5 mol Fe和足量浓硝酸混合,转移电子数为1.5NA
D. 0.1 mol H2和0.1 mol I2 (g)于密闭容器中充分反应,其原子总数为0.2NA
【答案】A
【解析】
A. D2O和H2l8O的摩尔质量相同都为20g/mol,中子数也相等均为10,所以2gD2O和H2l8O混合物中所含中子数为NA,故A正确;B. NaHCO3属于强碱弱酸盐,HCO3-既能发生电离:HCO3-![]() H++CO32-,也能发生水解:H2O+HCO3-
H++CO32-,也能发生水解:H2O+HCO3-![]() H2CO3+OH-,根据物料守恒可知,1L0.1mol·L-1 NaHCO3溶液中H2CO3、HCO3-和CO32-离子数之和为0.1NA,故B错误。C. 常温常压下, Fe和足量浓硝酸发生钝化反应,故C错误;D. 0.1 mol H2和0.1 mol I2 (g)于密闭容器中充分反应为H2(g)+I2 (g)
H2CO3+OH-,根据物料守恒可知,1L0.1mol·L-1 NaHCO3溶液中H2CO3、HCO3-和CO32-离子数之和为0.1NA,故B错误。C. 常温常压下, Fe和足量浓硝酸发生钝化反应,故C错误;D. 0.1 mol H2和0.1 mol I2 (g)于密闭容器中充分反应为H2(g)+I2 (g)![]() 2HI,其原子总数为0.4NA,故D错误;答案:A 。
2HI,其原子总数为0.4NA,故D错误;答案:A 。


科目:高中化学 来源: 题型:
【题目】参照反应Br+H2→HBr+H的能量随反应历程变化的示意图,下列叙述中正确的是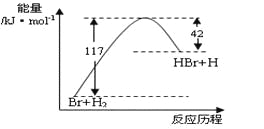
A. 反应物具有的总能量大于生成物具有的总能量
B. 正反应为吸热反应
C. 该反应的逆反应是吸热过程
D. 图中可以看出,HBr的能量一定高于H2的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,800 ℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是
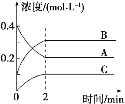
A. 发生的反应可表示为2A(g)![]() 2B(g)+C(g)
2B(g)+C(g)
B. 前2 min A的分解速率为0.1 mol/(L·min)
C. 开始时,正、逆反应同时开始
D. 2 min时,A、B、C的浓度之比为2∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按第26届国际计量大会重新定义,阿伏加德罗常数(NA)有了准确值6.02214076×1023。下列说法正确的是
A. 18 gT2O中含有的中子数为12NA
B. 用23.5gAgI与水制成的胶体中胶体粒子数目为0.1NA
C. 标准状况下,2.24LCl2全部溶于水所得溶液中的Cl-数目为0.1NA
D. 1mol某烷烃CnH2n+2(n≥1)分子中含有的共价键数为(3n+1)NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A是一种重要的化工原料,合成路线如下:
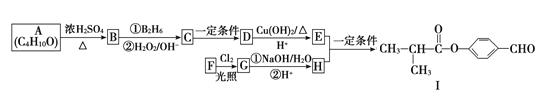 已知以下信息:
已知以下信息:
①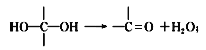
② R—CH===CH2![]() R—CH2CH2OH;
R—CH2CH2OH;
③核磁共振氢谱显示A有2种不同化学环境的氢。
(1)A 的名称是________。F的结构简式为________。
(2)A―→B的反应类型为________。I中存在的含氧官能团的名称是________。
(3)写出下列反应的化学方程式。
D―→E:__________。
(4)I的同系物J比I相对分子质量小28,J的同分异构体中能同时满足如下条件的共有________种(不考虑立体异构)。
①苯环上只有两个取代基;②既含-CHO,又能和饱和NaHCO3溶液反应放出CO2
(5)参照上述合成路线,以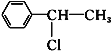 为原料(无机试剂任选),设计制备苯乙酸(
为原料(无机试剂任选),设计制备苯乙酸(![]() )的合成路线:__________________________
)的合成路线:__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以柏林绿Fe[Fe(CN)6]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列说法正确的是
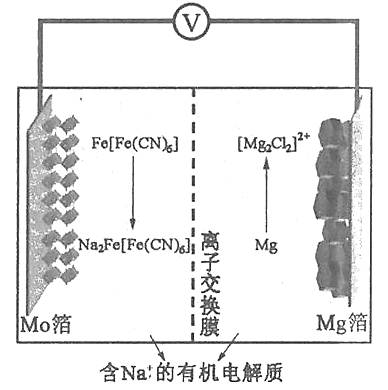
A. 放电时,Mo箔上的电势比Mg箔上的低
B. 充电时,Mo箔接电源的负极
C. 放电时,正极反应为Fe[Fe(CN)6]+2Na++2e-=Na2Fe[Fe(CN)6]
D. 充电时,外电路中通过0.2mol电子时,阴极质量增加3.55g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,反应CO+H2O![]() CO2+H2 达平衡。恒容时,温度升高,H2浓度减小。下列说法正确的是
CO2+H2 达平衡。恒容时,温度升高,H2浓度减小。下列说法正确的是
A. 该反应的焓变为负值
B. 恒温恒容下,增大压强,平衡一定不动
C. 升高温度,正反应速率减小
D. 平衡常数 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏加德罗常数) ( )
A. 124 g P4中含有P—P键的个数为4NA
B. 12 g石墨中含有C—C键的个数为1.5NA
C. 12 g金刚石中含有C—C键的个数为4NA
D. 60 g SiO2中含有Si—O键的个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L某溶液中含有的离子如下表:
离子 | Cu2+ | Al3+ | NO | Cl- |
物质的量浓度(mol·L-1) | 1 | 1 | a | 1 |
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是( )
A. 电解后溶液呈酸性 B. a=3
C. 阳极生成1.5 mol Cl2 D. 阴极析出的金属是铜与铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com