
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________。
(4
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式);呈两性的氢氧化物是_________(填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________。
【答案】Ca 离子键、共价键 ![]() r(Al3+)<r(Mg2+) <r(O2-)<r(N3-) HClO4 Al(OH)3 Al(OH) 3+OH-=AlO2-+2H2O
r(Al3+)<r(Mg2+) <r(O2-)<r(N3-) HClO4 Al(OH)3 Al(OH) 3+OH-=AlO2-+2H2O 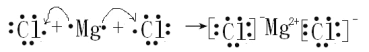
【解析】
根据元素周期表可知,①为Na、②为K、③为Mg、④为Ca、⑤为Al、⑥为C、⑦为N、⑧为O、⑨为Cl、⑩为Ar。
(1)③为Mg、④为Ca、⑤为Al、⑥为C、⑦为N,同周期,从左到右,原子半径减小,同主族,从上到下,原子半径增大,所以原子半径大小关系为:r(Ca)>r(Mg)>r(Al)r(C)>r(N),最大的是Ca,故答案为:Ca。
(2)⑦为N,其最高价氧化物对应的水化物式HNO3,其氢化物是NH3,二者反应生成NH4NO3,NH4NO3为离子化合物,NH4+与NO3-之间是离子键,NH4+与NO3-之内是共价键,所以含有的化学键类型有离子键、共价键,故答案为:离子键、共价键。
(3)①为Na、⑧为O,其单质在加热条件下反应生成Na2O2,Na2O2是离子化合物,其电子式为![]() ,故答案为:
,故答案为:![]() 。
。
(4)③为Mg、⑤为Al、⑦为N、⑧为O,形成Mg2+、Al3+、N3-、O2-,核外电子层结构相同的离子,核电荷数越大,离子半径越小,其半径由小到大的顺序是r(Al3+)<r(Mg2+) <r(O2-)<r(N3-),故答案为:r(Al3+)<r(Mg2+) <r(O2-)<r(N3-)。
(5)①为Na、②为K、③为Mg、④为Ca、⑤为Al、⑥为C、⑦为N、⑧为O、⑨为Cl,同周期,从左到右,最高价氧化物对应的水化物中酸性增强,同主族,从上到下,最高价氧化物对应的水化物中酸性减弱,所以酸性最强的是HClO4;呈两性的氢氧化物是Al(OH)3;Al(OH)3与NaOH溶液反应生成偏铝酸钠和水,其离子方程式为:Al(OH) 3+OH-=AlO2-+2H2O,故答案为:HClO4;Al(OH)3;Al(OH) 3+OH-=AlO2-+2H2O。
(6)③为Mg、⑨为Cl,Mg最外层有2个电子,易失去2个电子,Cl最外层有7个电子,易得到1个电子,二者形成MgCl2,用电子式表示其形成化合物的过程为:![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中不正确的是
A. 14g由N2和13C2H2组成的混合物中,所含中子数为7NA
B. CH4与白磷(P4)都为正四面体结构,则1mol CH4与lmolP4所含共价键的数目均为4NA
C. 反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4kJ/mol,若放出热量4.62kJ,则转移电子的数目为0.3NA
2NH3(g) ΔH=-92.4kJ/mol,若放出热量4.62kJ,则转移电子的数目为0.3NA
D. 常温下,含0.5molNH4NO3与xmolNH3·H2O的中性溶液中,含有NH4+的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)12.4g Na2X含有0.4mol Na+,Na2X的摩尔质量为_____,X的相对原子质量为_____。
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍.则X的相对原子质量为_____。
(3)0.05mol 的硫酸钠中含有_____个氧原子;与_____g NaCl中所含有的Na+数目相同.
(4)气态化合物A的化学式可以表示为OxFy,已知同温同压下10mLA受热完全分解生成15mLO2和10mL F2,则A的化学式为_____。
(5)0.5L 0.5mol/L FeCl3溶液中的Cl﹣的物质的量浓度为_____。
(6)质量分数为98%,密度为1.84g.cm﹣3的某浓硫酸,溶质的物质的量浓度为_____。
(7)a个X原子的总质量为b g,则X的相对原子质量可表示为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁的电化学腐蚀原理如图所示,下列有关说法中错误的是( )
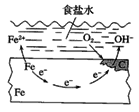
A. 铁片里的铁和碳与食盐水形成无数的微小原电池
B. 铁电极发生氧化反应
C. 负极的电极反应方程式为O2+4e-+2H2O=4OH-
D. 放置一段时间后,铁片上有铁锈出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L密闭容器中充入4molA气体和3molB气体,发生下列反应:2A(g)+B(g) ![]() C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。
C(g)+xD(g),5s达到平衡。达到平衡时,生成了1mol C,测定D的浓度为1mol/L。
(1)求x =____。
(2)求这段时间A的平均反应速率为_____。
(3)平衡时B的浓度为______。
(4)下列叙述能说明上述反应达到平衡状态的是_____
A 单位时间内每消耗2 mol A,同时生成1molC
B 单位时间内每生成1molB,同时生成1mol C
C D的体积分数不再变化
D 混合气体的压强不再变化
E B、C的浓度之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4=ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则其能量转化形式为电能转化为化学能
D. 若将其设计为原电池,当有32.5gZn溶解时,正极放出的气体一定为11.2L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组化合物中,化学键类型和化合物类型均相同的是_________(填序号)。
A.CaCl2和 Na2S B.Na2O 和 Na2O2
C.CO2和CaO D.HC1 和 NaOH
(2)已知1 mol石墨转化为1 mol金刚石要吸收能量,则1 mol石墨的能量比1 mol金刚石的能量____(填“高”或“低”),石墨比金刚石_______(填“稳定”或“不稳定”)。
(3)Ba(OH)2 8H2O和NH4Cl反应的化学方程式是____________,该反应是___(填“吸热”或“放热”)反应,反应过程能量变化的图像符合_____________(填“图1”或“图2”)。
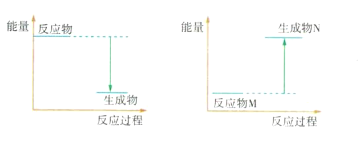
图1 图2
(4)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是___________________________。
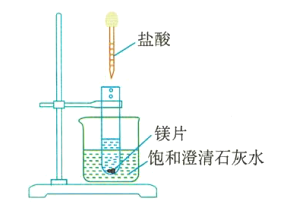
图3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国核物理研究所的科学家实验发现,植物和落叶都能产生甲烷,其生成随着温度和日照的增强而增加。甲烷(CH4 )在足量O2中完全燃烧产生CO2和H2O(g) ,该反应中各物质所含化学键键能如图所示(键能是气态基态原子形成1 mol化学键释放的最低能量,单位为kJ·mol 1)。下列说法错误的是

A.甲烷在氧气中燃烧的反应为放热反应
B.O=O键的键能比C=O键的键能小
C.1 mol甲烷在足量氧气中燃烧产生的H2O(g)所含化学键的能量为1856 kJ
D.1 mol CH4所含化学键的能量比1 mol CO2所含化学键的能量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学将铁铝合金样品溶解后取样 25.00 mL,分离并测定Fe3+的浓度,实验方案设计如下:

已知:乙醚[(C2H5)2O] 沸点为 34.5℃,易挥发、易燃,不纯时点燃易发生爆炸,微溶于水,密度比水小。在盐酸浓度较高时,Fe3+与 HCl、乙醚形成化合物[(CH3 ) OH][FeCl ]而溶于乙醚;当盐酸浓度降低时,该化合物解离。请回答:
(1)操作A 得到溶液Ⅰ,具体操作是:静置后,_____________________________。
(2)经操作 A 后,为判断Fe3+是否有残留,请设计实验方案__________。
(3)蒸馏装置如图所示,装置中存在的错误是____________、______________。

(4)下列有关说法正确的是__________。
A.为了减少滴定误差,滴定管、锥形瓶均需用待装液润洗
B.标准KMnO4溶液应该装在酸式滴定管中
C.开始滴定前,滴定管标准液内有气泡,滴定终点时,气泡消失了,则测得Fe3+的浓度偏低
D.三次平行测定时,每次需将滴定管中的液面调至“0”刻度或“0”刻度以下的附近位置
(5)用 0.1000 mol·L-1 KMnO 4溶液进行滴定,平行 实验三次,达到终点时,平均消耗KMnO4溶液 6.00 mL (滴定前先除去溶液中溶解的 HCl)。根据该实验数据,试样 X 中c(Fe3+)为____________。(结果保留三位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com