
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 | |
| C. | 一种元素可能有多种氧化物,但同一化合价只对应一种氧化物 | |
| D. | 强氧化剂与强还原剂不一定能发生氧化还原反应 |
分析 A.铁离子的氧化性大于铜离子;
B.在氧化还原反应中,可能只有一种元素的化合价变化;
C.Na的氧化物有氧化钠、过氧化钠;
D.高锰酸钾为强氧化性,活泼金属单质为强还原剂,常温下不反应.
解答 解:A.铁离子的氧化性大于铜离子,但金属性Fe大于Cu,故A错误;
B.在氧化还原反应中,可能只有一种元素的化合价变化,如氯气与水的反应中只有Cl元素的化合价变化,故B错误;
C.Na的氧化物有氧化钠、过氧化钠,Na均为+1价,故C错误;
D.高锰酸钾为强氧化性,活泼金属单质为强还原剂,常温下不反应,还有浓硫酸与二氧化硫不反应,可知强氧化剂与强还原剂不一定能发生氧化还原反应,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握微粒的性质、常见反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意结合实例分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | FeS2$\stackrel{煅烧}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | NaCl(aq)$\stackrel{电解}{→}$Na$\stackrel{O_{2}}{→}$Na2O2 | |
| C. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq)$\stackrel{NaOH(aq)}{→}$Fe(OH)2$\stackrel{空气中灼烧}{→}$Fe2O3 | |
| D. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{Cu}{→}$Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①③⑤ | B. | ①② | C. | ②③⑤ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将饱和的FeCl3溶液滴入沸水中形成Fe(OH)3胶体 | |
| B. | CuSO4溶液可观察到丁达尔现象 | |
| C. | Fe(OH)3胶体可观察到丁达尔现象 | |
| D. | 胶体分散系中所有粒子的直径都不在1~100 nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚和甲醛在一定条件下可合成酚醛树脂 | |
| B. | 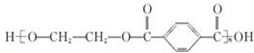 的单体是 HOCH2CH2OH 与 的单体是 HOCH2CH2OH 与  | |
| C. | 聚苯乙烯是由苯乙烯加聚生成的纯净物 | |
| D. | 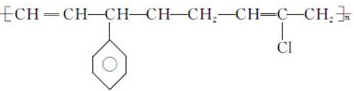 的单体有3种 的单体有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol•L-1的HCl溶液 | B. | 1 mol•L-1的KCl溶液 | ||
| C. | 0.8 mol•L-1的AlCl3溶液 | D. | 0.5 mol•L-1的FeCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水溶液和熔融状态下能导电的化合物,叫做电解质 | |
| B. | 在水溶液或熔融状态下能导电的化合物,叫做电解质 | |
| C. | BaSO4是难溶物,所以是非电解质 | |
| D. | 氧化还原反应的本质是化合价升降 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
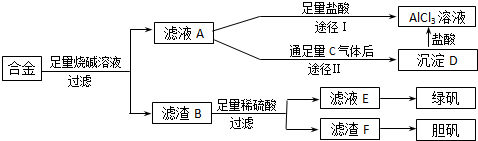
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com