
| m |
| M |
| 6.4g×188 |
| 64 |
| 6.4g |
| 64g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、NH4+ |
| B、NO2 |
| C、NO |
| D、N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
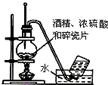 | 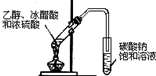 | 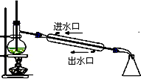 | 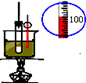 |
| A.实验室用乙醇制取乙烯 | B.实验室制取乙酸乙酯 | C.石油分馏 | D.实验室制取硝基苯 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如图所示,则:
M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如图所示,则:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com