
华素片(西地碘片)使用说明书 【品名和组成】 品名:西地碘片 组成:华素片 英文名:Cydiodine Tablets 华素片(西地碘片)的主要活性成分是分子碘,含量1.5 mg/片。将碘利用分子分散技术制成分子态西地碘,并含适量薄荷脑等 【贮藏】 遮光、密闭、在凉处保存 【有效期】 二年 |
(1)根据上述说明和所学知识回答:
①华素片中含有的活性成分是______________(写分子式)。
②请推断华素片______________(“是”或“不是”)白色。
(2)某学生为验证华素片中确实含有上述成分,完成实验如下,请填空:
①取一粒药片放入研钵中研碎,再将药粉装入试管并加入约2 mL蒸馏水;向试管中再加入约2 mL______________(填选项字母),并用力振荡。
A.酒精(密度比水小,与水任意比混溶)
B.四氯化碳(密度比水大,不溶于水)
②描述加入该液体后可能观察到的现象________________________________。
③选用该液体的原因是________________________________________。
(3)请再设计另一种方法,验证华素片中的成分(注意叙述实验原理,操作方法和实验结论)________________________________。
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||


| ||
| ||
查看答案和解析>>
科目:高中化学 来源:必修一导学指导化学鲁科版 鲁科版 题型:058
某学习小组收集了关于卤素在生活中的应用资料.其中有一份是药物华素片(西地碘片)的使用说明书,以下为说明书的部分内容:
(1)根据上述说明和所学知识回答:
①华素片中含有的活性成分是________(写分子式).
②请推断华素片________(“是”或“不是”)白色.
(2)某学生为验证华素片中确实含有上述成分,完成实验如下,请填空:
①取一粒药片放入研钵中研碎,再将药粉装入试管并加入约2 mL蒸馏水;向试管中再加入约2 mL________(填选项字母),并用力振荡.
A.酒精(密度比水小,与水任意比混溶)
B.四氯化碳(密度比水大,不溶于水)
②描述加入该液体后可能观察到的现象________.
③选用该液体的原因是________.
(3)请再设计另一种方法,验证华素片中的成分(注意叙述实验原理,操作方法和实验结论)_________________________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市高三第二次月考化学试卷(解析版) 题型:实验题
(18分)
Ⅰ. 氨是一种重要的化工原料,某学习小组欲制取氨气并探究其性质。
请回答:
(1)实验室制取氨气的化学方程式是 。
(2)① 如图是进行氨气喷泉实验的装置,引发喷泉的操作步骤是 。

② 氨气使烧杯中溶液由无色变为红色,其原因是(用电离方程式表示) 。
(3)该小组同学设计了下图所示的实验装置(部分夹持仪器未画出),探究氨气的还原性并检验产物。
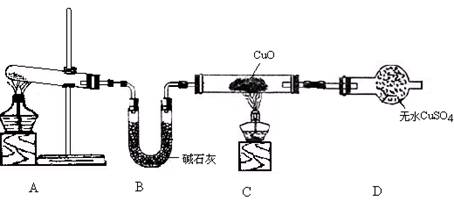
① 实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式 。
② 碱石灰的作用是 。
③ 整套装置在方框处应添加一种装置后,此实验设计才较完善,请在方框中补画出E装置图(要求注明装置中所加试剂名称)。

Ⅱ. 3.2g Cu与30mL,8mol/L过量HNO3反应,硝酸的还原产物为NO,NO2,反应后溶液中所含H+为a mol,则:①此时溶液中所含的NO3-为 mol。
②所生成的NO在标准状况下体积为 L。(以上结果均用含a的代数式表示)
Ⅲ. 某黑色固体甲可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料知道:①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。②硫化铜和硫化亚铜常温下都不溶于稀盐酸。在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图所示的实验:
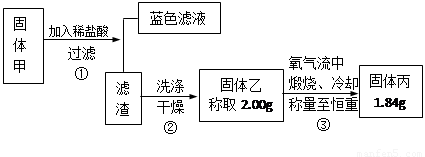
(1)③中在煅烧过程中一定发生的反应的化学方程式为 。
(2)关于固体甲的成分的判断中,下列说法正确的是
A.固体甲中,CuS和Cu2S不能同时存在;
B.固体甲中,CuO和Cu2O至少有一种;
C.固体甲中若没有Cu2O,则一定有Cu2S;
D.固体甲中若存在Cu2O,也可能有Cu2S。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年天津市大港一中高三(上)第二次月考化学试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com