
实验室使用的浓盐酸的溶质质量分数一般为36.5%,密度1.19g/cm3.
(1)将 升氯化氢(标准状况)通入1.00L水中可以得到36.5%的浓盐酸?
(2)该浓盐酸的物质的量浓度为 .
考点:
溶液中溶质的质量分数及相关计算;物质的量浓度的相关计算.
专题:
物质的量浓度和溶解度专题.
分析:
(1)令需要氯化氢的体积为VL,根据n= 计算HCl的物质的量,再根据m=nM计算HCl的质量,根据m=ρV计算水的质量,进而计算溶液的质量,再根据质量分数列方程计算;
计算HCl的物质的量,再根据m=nM计算HCl的质量,根据m=ρV计算水的质量,进而计算溶液的质量,再根据质量分数列方程计算;
(2)根据c=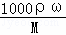 计算该盐酸的物质的量浓度.
计算该盐酸的物质的量浓度.
解答:
解:(1)令需要氯化氢的体积为VL,则HCl的物质的量为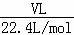 =
= mol,故HCl的质量为
mol,故HCl的质量为 mol×36.5g/mol=
mol×36.5g/mol= g,1.00L水的质量为1L×1000g/L=1000g,故溶液的质量为(1000+
g,1.00L水的质量为1L×1000g/L=1000g,故溶液的质量为(1000+ )g,故(1000+
)g,故(1000+ )g×36.5%=
)g×36.5%=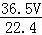 g,解得:V=352.8L,
g,解得:V=352.8L,
故答案为:352.8;
(2)质量分数为36.5%,密度1.19g/cm3的浓盐酸的物质的量浓度为 mol/L=11.9mol/L,
mol/L=11.9mol/L,
答:该浓盐酸的物质的量浓度为11.9mol/L.
点评:
考查质量分数、物质的量浓度的有关计算,难度中等,理解概念是解题的关键,注意常用化学计量的计算.


科目:高中化学 来源: 题型:
下列溶液一定呈中性的是( )
A.pH=7的溶液
B.[H+]=[OH-]的溶液
C.由强酸、强碱等物质的量反应得到的溶液
D.非电解质溶于水得到的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列反应判断有关物质还原性由强到弱的顺序是( )
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
|
| A. | H2SO3>I﹣>Fe2+>NO | B. | I﹣>Fe2+>H2SO3>NO |
|
| C. | Fe2+>I﹣>H2SO3>NO | D. | NO>Fe2+>H2SO3>I﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
现在要分离下列物质,请根据分离实例,将合适的分离方法填在后面的直线上.
(1)要除去NaCl溶液中的泥沙
(2)用CCl4提取溴水中的溴单质
(3)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)
(4)分离汽油和水
(5)从含有少量NaCl的KNO3溶液中提取KNO3
(6)分离Fe(OH)3胶体中含有的FeCl3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体物质只含有钠和氧两种元素,将它放在足量的水中产生两种气体,这两种气体又可以在一定条件下反应生成水,则原固体物质的组成是( )
A.Na2O2与Na2O B.Na和NaOH
C.Na2O2和Na D.Na和Na2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:
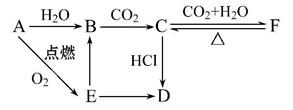
(1)写出A、B、C、D、E、F的化学式:
A. ;B. ;C. ;
D. ;E. ;F. 。
(2)写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
B C: ___________________________________________________,
C: ___________________________________________________,
E B: __________________________________________________,
B: __________________________________________________,
C F: __________________________________________________,
F: __________________________________________________,
F C: __________________________________________________。
C: __________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
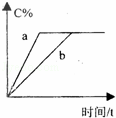
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)⇌2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
|
| A. | a的温度高于b | B. | a使用了催化剂,而b未用 |
|
| C. | a的压强大于b | D. | a的温度低于b |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于氧化还原反应的是( )
|
| A. | CaO+H2O=Ca(OH)2 | B. | NaCl+AgNO3=NaNO3+AgCl↓ |
|
| C. | H 2CO3=H2O+CO2↑ | D. | H2+CuO=Cu+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com