
运用相关化学知识进行判断,下列结论错误的是( )
A.某吸热反应能自发进行,因此该反应是熵增反应
B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
D.增大反应物浓度可加快 反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
科目:高中化学 来源: 题型:
下列有关食品添加剂的说法正确的是
A.需要长时间储存的食品应加入适宜的防腐剂
B.冰激凌不使用着色剂营养价值一定会降低
C.色、香、味俱全的食物营养价值不一定高
D. 炒菜时拒绝添加食盐、味精等各种调味剂
查看答案和解析>>
科目:高中化学 来源: 题型:
有0.1 mol/L Na2SO4溶液300 mL,0.1 mol/L MgSO4溶液200 mL和0.1 mol/L Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是( )
A.1∶1∶1 B.3∶2∶2 C. 3∶2∶3 D.1∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
新型净水剂高铁酸钠(Na2FeO4)可通过以下反应制备:
Fe2O3+3Na2O2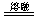 2Na2FeO4+Na2O,下列说法正确的是( )
2Na2FeO4+Na2O,下列说法正确的是( )
A.Na2O2既是氧化剂又是还原剂
B.Na2FeO4既是氧化产物又是还原产物
C.在Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒
D.3 mol Na2O2发生反应,有12 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题。
(1)上述实验中发生反应的化学方程式有_______________________________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是_________________________________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO 4溶液起相似作用的是________。
4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有______________________(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 |
| V5 |
| 饱和CuSO4 溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=________,V6=________,V9=________。
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色。
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
大气中的部分源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)===IO-(aq)+O2(g) ΔH1;
②IO-(aq)+H+(aq)  HOI(aq) ΔH2;
HOI(aq) ΔH2;
③HOI(aq)+I-(aq)+H+(aq)  I2(aq)+H2O(l) ΔH3。
I2(aq)+H2O(l) ΔH3。
总反应的化学方程式为______________________________________________________,其反应热ΔH=________。
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)  I
I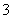 (aq),其平衡常数表达式为______________。
(aq),其平衡常数表达式为______________。
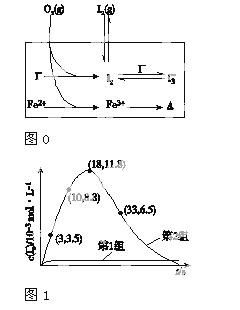
(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图0),某研究小组测定两组实验中I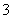 浓度和体系pH,结果见图1和下表。
浓度和体系pH,结果见图1和下表。
| 编号 | 反应物 | 反应前pH | 反应后pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2+ | 5.2 | 4.1 |
①第1组实验中,导致反应后pH升高的原因是__________________________________
________________________________________________________________________。
②图中的A为________。由Fe3+生成A的过程能显著提高I-的转化率,原因是
________________________________________________________________________
________________________________________________________________________。
③第2组实验进行18 s后,I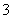 浓度下降。导致下降的直接原因有(双选)________。
浓度下降。导致下降的直接原因有(双选)________。
A.c(H+)减小 B.c(I-)减小
C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图1,计算3~18 s内第2组实验中生成I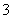 的平均反应速率(写出计算过程,结果保留两位有效数字)。
的平均反应速率(写出计算过程,结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于催化剂的说法不正确的是 ( )
A.温度越 高,催化剂的催化效果越好
高,催化剂的催化效果越好
B.汽车排气管上的“催化转化器”能减少有害气体排放
C.催化剂可以改变化学反应速率,但反应前后质量和化学性质不变
D.锌与盐酸反应时,加入几滴硫酸铜溶液可加快化学反应速率,但硫酸铜不作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定温度下,难溶化合物饱和溶液的离子浓度的乘积为一常数,这个常数用
在一定温度下,难溶化合物饱和溶液的离子浓度的乘积为一常数,这个常数用 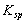 表示。已知:
表示。已知: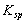 (AgCl) = = 1.8×10-10;
(AgCl) = = 1.8×10-10;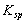 (Ag2CrO4) = 2 = 1.9×10-12
(Ag2CrO4) = 2 = 1.9×10-12
现有0.001 mol·L-1 AgNO3溶液滴定0.001 mol·L-1 KCl和0.001 mol·L-1 的K2CrO4的混和溶液,试通过计算回答:
(1)Cl-和CrO42- 哪种先沉淀?
(2)当CrO42- 以 Ag2CrO4 形式沉淀时,溶液中的Cl- 离子浓度是多少? CrO42- 与Cl- 能否达到有效的分离?(设当一种离子开始沉淀时,另一种离子浓度小于10-5 mol·L-1 时,则认为可以达到有效分离)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值,下列说法正确的是 ( )
A.0.1molN2与0.3molH2在密闭容器催化剂作用下充分反应,生成氨分子数为0.2NA
B.标准状况下,11.2L甲醛气体中电子数为8NA
C.常温常压下,7.8g苯中含有单键的数目为0.9NA
D.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com