
【题目】有A、B、C、D四种元素,A的最高正价与其最低负价的绝对值之差为6;A、D次外层都是8个电子,A与D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B有两个电子层,其最高正价与最低负价的代数和为0;C2-与氩原子具有相同的电子层结构。
(1)试写出上述各元素的符号:A______,B______,C______,D______。
(2)画出下列粒子的结构示意图:A:________________,C2-:__________。
(3)元素A、C、D形成简单离子的半径由大到小的顺序是________________。
(4)写出A、D的最高价氧化物对应水化物反应的化学方程式:_____________。
【答案】Cl C S K ![]()
![]() S2->Cl->K+ HClO4+KOH=KClO4+H2O
S2->Cl->K+ HClO4+KOH=KClO4+H2O
【解析】
A、B、C、D四种元素,C2-离子与氩原子具有相同的电子层结构,则C为硫元素;B有两个电子层,其最高正化合价与最低负化合价的代数和为零,则最外层电子数为4,故B为碳元素;A的最高正价与其最低负价的代数和为6,则A处于ⅦA族,A次外层电子数是8个,则A为氯元素;D次外层电子数是8个,A和D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子,A为氯元素,A离子带1个单位负电荷,核外电子数为18,所以D的阳离子带1个单位正电荷,核外电子数为18,故D为钾元素,据此分析。
(1)由上述分析可知A元素符号为Cl;B元素符号为C;C元素符号为S;D元素符号为K;
(2)A为氯原子,其结构示意图为![]() ;C2-为硫离子,是硫原子得到两个电子,最外层达到8电子稳定结构,其离子结构示意图为
;C2-为硫离子,是硫原子得到两个电子,最外层达到8电子稳定结构,其离子结构示意图为![]() ;
;
(3)A为Cl;C为S;D为K,故离子具有相同的核外电子排布,根据核电荷数越大的,离子半径反而小可得离子半径由大到小的顺序为S2->Cl->K+。
(4)A、D的的最高价氧化物对应水化物为HClO4、KOH,反应的化学方程式为HClO4+KOH=KClO4+H2O。


科目:高中化学 来源: 题型:
【题目】葡萄糖酸锌是一种常见的补锌药物,常用葡萄糖酸和![]() 反应制备。
反应制备。
(1)![]() 基态核外电子排布式为________。
基态核外电子排布式为________。
(2)![]() 的空间构型为________(用文字描述);
的空间构型为________(用文字描述);![]() 与
与![]() 反应能生成
反应能生成![]() ,不考虑空间构型,
,不考虑空间构型,![]() 的结构可用示意图表示为________。
的结构可用示意图表示为________。
(3)葡萄糖酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为________;推测葡萄糖酸在水中的溶解性:________(填“难溶于水”或“易溶于水”)。

(4)用![]() 可以制备
可以制备![]() ,一个
,一个![]() 晶胞(如图2)中,
晶胞(如图2)中,![]() 的数目为________。
的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一位学生设计的实验室制取和收集氯气并验证其性质的装置图。
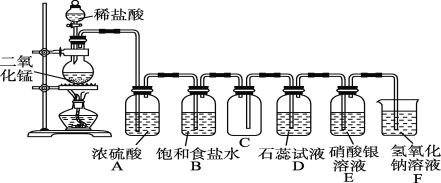
(1)找出在此装置图中出现的错误并加以改正:___。
(2)实验过程中,在D装置中观察到的实验现象是___;在E装置中观察到的实验现象是___,反应的化学方程式是____。
(3)F装置的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g) △H=-197 kJ·mol-1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g) △H=-197 kJ·mol-1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是
A. 若c(SO2)与c(O2)之比为k,则:k甲=k丙>k乙
B. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
C. 容器内压强P:P甲=P丙>2P乙
D. SO3的质量m:m甲=m丙>2m乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ·mol-1。
(1)写出甲醚燃烧的热化学方程式____;已知H2(g)和C(s)的燃烧热分别是285.8kJ·mol-1、393.5kJ·mol-1;计算反应:4C(s)+6H2(g)+O2(g)=2CH3OCH3(g)的反应热为____。
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g)△H<0
CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是____
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1molH2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将___(填“变大”、“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列与溶液pH有关的计算
(1)室温下pH=2的HCl溶液和pH=10的NaOH溶液中由水电离出的c(H+)之比为____。
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后,溶液中的氢离子浓度为__。
(3)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得混合溶液pH=3,则a:b=___。
(4)已知某温度时0.1molL-1NaOH pH等于11,在此温度下,若将100体积pH1=a的H2SO4溶液与1体积pH2=b的NaOH溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是___(用含a、b的表达式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液:Na+、Cu2+、NO3-、Cl-
B.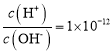 的溶液:K+、Na+、CO32-、NO3-
的溶液:K+、Na+、CO32-、NO3-
C.使甲基橙呈红色的溶液:Ba2+、NH4+、Cl-、ClO-
D.能溶解Al(OH)3的溶液:Na+、NH4+、NO3-、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图所示的转化关系中,![]() 、
、![]() 均为常见的金属单质;A、
均为常见的金属单质;A、![]() 在冷的
在冷的![]() 的浓溶液中均会发生钝化;
的浓溶液中均会发生钝化;![]() 为淡黄色的非金属单质。
为淡黄色的非金属单质。![]() 为红棕色固体氧化物,
为红棕色固体氧化物,![]() 为常见无色液体。
为常见无色液体。![]() 焰色为黄色,且能使酚酞变红(部分反应条件、反应过程中生成的水及其他产物略去)。
焰色为黄色,且能使酚酞变红(部分反应条件、反应过程中生成的水及其他产物略去)。

(1)![]() 的化学式为______。
的化学式为______。
(2)![]() 与
与![]() 反应的化学方程式为_____。
反应的化学方程式为_____。
(3)![]() 与氯气反应的离子方程式为_____。
与氯气反应的离子方程式为_____。
(4)![]() 与氨水反应的化学方程式为_______。
与氨水反应的化学方程式为_______。
(5)![]() 与
与![]() 反应的离子方程式为________。
反应的离子方程式为________。
(6)检验“黄色溶液”中阳离子的方案:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500~600 ℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。
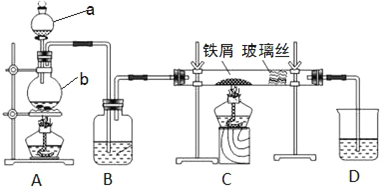
(1)写出仪器的名称:a_______,b________。
(2)A中反应的化学方程式为________。C中反应的化学方程式为________。
(3)装置B中加入的试剂是________。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置__和__(填字母)间增加一个盛有________的洗气瓶。
(5)装置D的作用是________。为防止水蒸气影响无水氯化铁的制取,请你提出一个对装置D的改进方案:________。
(6)反应结束后,取少量装置C中的固体于试管中,加入足量盐酸,固体完全溶解,得到溶液X。证明溶液X中含有FeCl3的试剂是________,观察到的现象是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com