
【题目】下列变化需克服相同类型作用力的是( )
A.碘和干冰的升华
B.硅和冰的熔化
C.氯化氢和氯化钾的溶解
D.氯化钠和冰融化
科目:高中化学 来源: 题型:
【题目】化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
(1)已知:FeO(s)+CO(g)FeO(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如右表:
T(K) | 938 | 1100 |
K | 0.68 | 0.40 |
①该反应平衡常数的表达式是 .
②在体积固定的密闭容器中该反应达到平衡状态后,升高温度混合气体的平均相对分子质
量(填“增大”、“减小”或“不变”)曰该反应正反应是反应(填“吸热”或“放热”).
(2)常温下,下列溶液的浓度均为0.1molL﹣1 , 测得溶液pH值如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
①由表中数据分析,上述溶质中的阴离子水解程度最小的是(填离子符号).
②由表中数据分析,0.01molL﹣1的下列溶液,酸性最弱的是(填编号).
A、H2CO3 B、HClO C、C6H5OH D、CH3COOH
③向氯水中加入少量的碳酸钠,可以增加氯水中HClO的浓度.为什么? . (请结合化学反应简要说明)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.实验室制备Cl2可用排饱和食盐水集气法收集
C.液氯、氯水均为含多种分子和离子的混合物
D.1.12 L Cl2含有1.7NA个质子(NA表示阿伏加德罗常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质均属于分子晶体且均为化合物的是( )
A.NH3、HD、C10H8B.PCl3、CO2、AlCl3
C.SO2、SiO2、P2O5D.CCl4、H2O2、Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H2S溶液中,c(H+)=c(HS﹣)=1×10﹣5molL﹣1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH﹣)+c(HC2O4﹣)
D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为反应2X(g)+Y(s)2Z(g)的反应过程和能量关系图,下列说法正确的是( ) 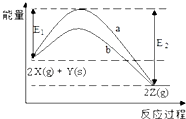
A.曲线a和b表示两个反应过程的反应热不同
B.曲线a一定表示反应是在无催化剂时的反应过程
C.增大压强,X的转化率一定增大
D.反应达平衡,升高温度,平衡常数K值一定减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com