
����Ŀ��̼�Ȼ�ԭ�Ȼ��������������������в����ԭ�������ʸߵ��ŵ㣬��ԭ�����£�
��Al2O3(s) + AlCl3(g) + 3C(s) ![]() 3AlCl(g) + 3CO(g) �C 1486 kJ
3AlCl(g) + 3CO(g) �C 1486 kJ
��3AlCl(g) ![]() 2Al(l) + AlCl3(g) + 140 kJ
2Al(l) + AlCl3(g) + 140 kJ
��1��д����Ӧ��Ļ�ѧƽ�ⳣ������ʽK=_____________�������¶ȣ�K_______��������С�����䣩��
��2��д����Ӧ��ﵽƽ��״̬��һ����־_________________________________����Ϸ�Ӧ����з�����AlCl3�����������е����ÿ��Կ���___________��
��3����1mol��������3mol��̿�Ļ�������2L��Ӧ�����У�����2mol AlCl3���壬�ڸ����·�����Ӧ����5min������������������27.6g����AlCl�Ļ�ѧ��Ӧ����Ϊ_________ mol/(L��min)��
��4��Na2O2���к�ǿ�������ԡ�����Na2O2��FeCl2��Һ�ܷ�����Ӧ��____Na2O2+ FeCl2+___H2O��____Fe(OH)3��+_____FeCl3+____NaCl����֪FeCl2ǰ��ϵ��Ϊ6����ƽ������ѧ����ʽ�����������ת�Ʒ������Ŀ________________���˷�Ӧ�б���ԭ��Ԫ����____________������������__________��
���𰸡�![]() ���� ѹǿ���� ���� 0.06
���� ѹǿ���� ���� 0.06  O Fe(OH)3��FeCl3
O Fe(OH)3��FeCl3
��������
������Ҫ����ƽ�ⳣ���ļ��㡢��ѧƽ����ƶ�������ԭ��Ӧ����д��
��1��![]() ����Kֵʱ�������������ʣ�����Ӧ���ȣ������¶ȷ�Ӧ���ƣ�
����Kֵʱ�������������ʣ�����Ӧ���ȣ������¶ȷ�Ӧ���ƣ�
��2����Ӧ��ﵽƽ��״̬��һ����־��Ҫ˵�����淴Ӧ������ͬ����Ӧǰ����������仯������
��3��AlCl�Ļ�ѧ��Ӧ����Ϊ![]() ͨ������ʽ���㣻
ͨ������ʽ���㣻
��4��Na2O2��FeCl2����������ԭ��Ӧͨ����ʧ�����غ��Ԫ�������غ���ƽ����ʽ��
��1��![]() ��ѧƽ�ⳣ��
��ѧƽ�ⳣ��![]() ������Ӧ���ȣ������¶ȷ�Ӧ����Kֵ���ʴ�Ϊ��
������Ӧ���ȣ������¶ȷ�Ӧ����Kֵ���ʴ�Ϊ��![]() ������
������
��2��![]() ����Ӧǰ����������仯����ѹǿ����˵����Ӧ�ﵽƽ��״̬����Ϸ�Ӧ����з�����AlCl3�����������в��뷴Ӧ���̣���������ɣ������ÿ��Կ����������ã��ʴ�Ϊ��ѹǿ���䣻������
����Ӧǰ����������仯����ѹǿ����˵����Ӧ�ﵽƽ��״̬����Ϸ�Ӧ����з�����AlCl3�����������в��뷴Ӧ���̣���������ɣ������ÿ��Կ����������ã��ʴ�Ϊ��ѹǿ���䣻������
��3��![]() ������3molAlCl��Ӧǰ��������������138g����5min������������������27.6g������õ����ɵ�AlCl���ʵ���
������3molAlCl��Ӧǰ��������������138g����5min������������������27.6g������õ����ɵ�AlCl���ʵ���![]() ��AlCl�Ļ�ѧ��Ӧ����
��AlCl�Ļ�ѧ��Ӧ����
![]() ���ʴ�Ϊ��0.06��
���ʴ�Ϊ��0.06��
��4��Na2O2��FeCl2��Һ�ܷ�Ӧ��Na2O2Ϊ����������O����ԭ��FeCl2Ϊ��ԭ����Fe(OH)3��FeCl3Ϊ�������FeCl2ǰ��ϵ��Ϊ6�ϼ�����6�ۣ��ɵ�ʧ�����غ��֪Na2O2ǰ��ϵ��Ϊ3���ٸ���ԭ���غ����ƽ����
 ���ʴ�Ϊ��
���ʴ�Ϊ��
 �� O;Fe(OH)3��FeCl3��
�� O;Fe(OH)3��FeCl3��


 ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
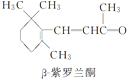
����Ŀ����������ͪ�Ǵ�����õ�廨�����ѵ��е�һ����Ȼ���ϣ������ಽ��Ӧ�ɺϳ�ά����A1������˵����ȷ����
 ��������
�������� ��������
��������
A.��������ͪ������ʵ�����Br2�ӳɷ�Ӧ������2�ֲ���
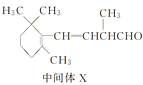
B.1 mol�м���X�������2 mol H2�����ӳɷ�Ӧ
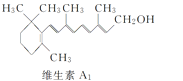
C.ά����A1������NaOH��Һ
D.��������ͪ���м���X��Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��װ�ý��е�ʵ�飬�ܴﵽ��Ӧʵ��Ŀ�ĵ��ǣ� ��
A.ͼ2���ռ�NO2����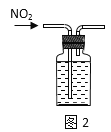
B.ͼ3����֤X��ҺΪŨ����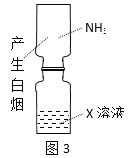
C.ͼ4����֤������ˮ�е��ܽ���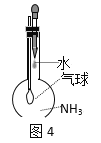
D.ͼ5����������β��NH3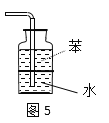
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ����٤������������˵����ȷ���ǣ� ��
A.�ڷ�Ӧ������0.1molCl2��ת�Ƶĵ�����һ��Ϊ0.2NA
B.15gCH3+��̼�����ӣ��к��еĵ�����Ϊ8NA
C.��״���£�11.2L��Ȳ�к����õ��ӶԵ���ĿΪ1.5NA
D.0.1L 2mol/L��(NH4)2S��Һ�к��е�S2-��ĿΪ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�ÿ������ķϾ�Ǧ����Լ330��֡��Ӻ�Ǧ���ϣ���PbSO4��PbO2��PbO�ȣ��л���Ǧ��ʵ��Ǧ�������������ش�һ�ֻ���Ǧ�Ĺ����������£�
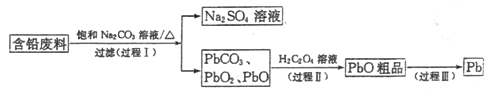
(1)Ǧ���طŵ�ʱ��PbO2��____����
(2)����I����֪��PbSO4��PbCO3���ܽ��(20��)��ͼl��Na2SO4��Na2CO3���ܽ�ȼ���ͼ��
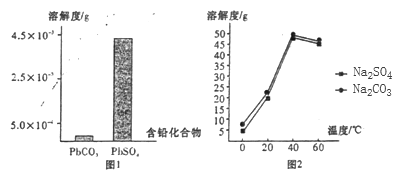
�ٸ���ͼlд������I�����ӷ���ʽ��__________��
�����������е��¶�Ӧ������40�棬���¶Ƚ��ͣ�PbSO4��ת�������½���������ͼ�����Ϳ���ԭ��
i���¶Ƚ��ͣ���Ӧ���ʽ��ͣ� ii��______________���������һ�ֺ������ͣ���
(3)�ٹ��̢�����Ӧ2PbO2+H2C2O4=2PbO+H2O2+2CO2����ʵ���м��д���O2�ų����Ʋ�PbO2������H2O2��ͨ��ʵ��֤ʵ����һ�Ʋ⡣ʵ�鷽����___________��
����֪��PbO2Ϊ�غ�ɫ���壻PbOΪ�Ȼ�ɫ���壩
��д��H2O2�ĵ���ʽ__________��
(4)���̢�PbO��Ʒ�ܽ���HCl��NaCl�Ļ����Һ�У��õ���Na2PbCl4�ĵ��Һ�����Na2PbCl4��Һ������Pb����ͼ��
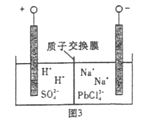
�������ĵ缫��Ӧʽ��____________��
�ڵ��һ��ʱ���PbCl42-Ũ�ȼ����½���Ϊ�˻ָ���Ũ����ʵ�����ʵ�ѭ�����ã���������ȡ�ķ�����_______��
��5�������Ǧ��������Դ��ⱥ��ʳ��ˮ��ȡCl2����֪ijǦ������������Һ�����Ϊ0.8L������䰴����Ũ��Ϊ4.5mol/L�����Ƶ�26.88L Cl2ʱ(ָ�ڱ�״����)���������ϵ�������������Һ��Ũ��Ϊ________ mol��L-1��(������ǰ��������Һ���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������õĽ���Ԫ�ء�����õķǽ���Ԫ�ء������³�Һ̬�Ľ���(�۵����Ų�Ϊ5d106s2)Ԫ�طֱ�λ������Ԫ�����ڱ��е�(����)
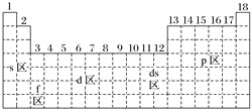
A. s����p����ds�� B. s����p����d��
C. f����p����ds�� D. s����f����ds��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж�ijδ֪��Һ�����ӵļ��鷽���������һ����ȷ����(����)
A.����ϡ���������ɫ���壬һ������![]()
B.�����Ȼ�����Һ������ɫ������һ������![]()
C.����̼������Һ������ɫ������һ������Ca2��
D.ȡ��Һ������ɫ��Ӧ�Ի�ɫ��һ������Na��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�ɷ�ΪFe2O3��Fe3O4���Լ�����SiO2��Al2O3�ȡ��������������Ʊ����죨Fe2O3����һ�ֹ����������£�

��֪����ԭ����ʱ����Fe2O3��Fe3O4ת��ΪFeO��
�������ӿ�ʼ��������ȫ����ʱ��pH���±���ʾ��
���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
Fe2+ | 7.6 | 9.7 |
Fe3+ | 2.7 | 3.7 |
Al3+ | 3.8 | 4.7 |
��1���������������������������Һ�еĽ����������У������ӷ��ţ�________________��
��2��Fe�۳���pH�⣬��һ��������___________��Fe�۵�����Һ��pHΪ__________��
��3��������������������������FeCO3�����ӷ���ʽΪ_______________________________��
������Һ����Ҫ�����ǣ��ѧʽ��_______________��
��4�����������£��������������з�����Ӧ�Ļ�ѧ����ʽΪ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��BaTiO3��KH2PO4��NaNO2�����������壬���Ǿ�����������������統����ѹ�����ı���״ʱ����������ͨ��ʱ��ı���״�ȡ�
(1)��̬Tiԭ�ӵļ۵����Ų�ʽΪ___________������___________��Ԫ�ء�
(2)KH2PO4�����д��ڵ���������___________(ѡ����ĸ)��
A.���Ӽ� B.���ۼ� C.���
(3) NaNO2��Nԭ�ӵ��ӻ�����Ϊ___������(�>��<��=��)____120�㣬��ԭ����___________��N��O��Na����Ԫ�صĵڶ�������(I2)�ɴ�С��˳��Ϊ________(��Ԫ�ط��ű�ʾ)��
(4)BaTiO3�ľ�������ͼ��ʾ��

Tiԭ�ӵ���λ��Ϊ_____��������ܶ�Ϊ��g/cm3�������Baԭ�Ӻ�Oԭ��֮��ľ���Ϊ___�������ʽ)nm��( BaTiO3��Ħ������Ϊ233g/mol��NAΪ�����ӵ�������ֵ)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com