
【题目】FeCl2是一种重要的污水处理剂,具有易与水反应、易被氧化的性质。某兴趣小组在实验室中制备无水FeCl2并测定其纯度,设计了如下实验(夹持装置已略去,I中各装置不重复使用)。
Ⅰ.FeCl2的制备
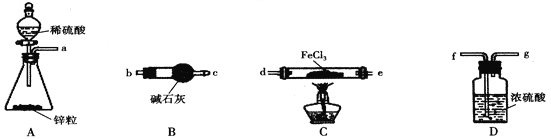
(1)加热条件下,H2与FeCl3制备无水FeCl2的化学方程式为______________________。
(2)按气流从左到右的方向,上图中装置合理的连接顺序为_________________(用仪器接口处的字母表示)。
(3)装置B的作用为____________。
(4)反应结束后,应先熄灭C处的酒精灯还是先关闭A处分液漏斗的活塞_______________(填“熄灭酒精灯”或“关闭活塞”)。
Ⅱ.FeCl2的纯度测定
已知:①实验得到固体的成分为FeCl2和FeCl3。
②Fe3+与K3[Fe(CN)6]不反应,3Fe2++2 [Fe(CN)6]3-![]() Fe3[Fe(CN)6]2↓。
Fe3[Fe(CN)6]2↓。
该兴趣小组设计了如下实验测定得到的FeCl2和FeCl3混合物中FeCl2的纯度。
(i)称取m g反应后的固体溶于过量盐酸中,再将所得溶液加水稀释到200 mL。
(ii)准确量取20 mL上述溶液于烧杯中,加入过量的K3[Fe(CN)6]溶液,有蓝色的Fe3[Fe(CN)6]2沉淀生成。
(iii)过滤、洗涤、干燥后进行称量,得到W g蓝色固体。
(5)产品中FeCl2的质量分数为____________________________(用含有m和ω的式子表示)。甲同学认为按照上述方案测得的FeCl2的质量分数偏低,他的理由为______________________
【答案】 2FeCl3+H2![]() 2FeCl2+3HCl afgde(ed)b(c) 吸收反应生成的氯化氢气体,防止其污染空气;防止空气中的水蒸气进入装置C与无水氯化亚铁反应 熄灭酒精灯 905w/296m×100% 在实验过程中会有部分FeCl2被空气中的氧气氧化为2FeCl3,使测得的w数值偏小,结果偏低
2FeCl2+3HCl afgde(ed)b(c) 吸收反应生成的氯化氢气体,防止其污染空气;防止空气中的水蒸气进入装置C与无水氯化亚铁反应 熄灭酒精灯 905w/296m×100% 在实验过程中会有部分FeCl2被空气中的氧气氧化为2FeCl3,使测得的w数值偏小,结果偏低
【解析】考查物质的制备和实验方案设计与评价,(1)H2与FeCl3反应制备FeCl2,Fe3+的化合价降低,H的化合价升高,转变为+1价,因此反应方程式为:2FeCl3+H2![]() 2FeCl2+3HCl;(2)首先是制气装置,即a开头,装置A中制备的氢气中含有水蒸气,连有干燥装置,根据制备FeCl2的反应方程式,有HCl的生成,HCl污染空气,应用碱石灰吸收,因此a连接f、g,g连接d、c或g连接c、d,d连接b,顺序是 afgde(ed)bc;(3)装置B的作用是吸收反应生成氯化氢气体,防止其污染空气,防止空气中的水蒸气进入装置C与无水氯化亚铁反应;(4)应先熄灭酒精灯,再通一段时间的氢气,让FeCl2冷却,防止被氧气氧化FeCl3;(5)根据反应方程式,求出Fe2+的物质的量为W×3/592mol,200mL的溶液中FeCl2的质量分数为W×3×127×200/(592×20)×100%=1905w/296m×100%,因为Fe2+容易被氧化,因此结果偏低的原因是:在实验过程中会有部分FeCl2被空气中的氧气氧化为FeCl3,使测得的w数值偏小,结果偏低。
2FeCl2+3HCl;(2)首先是制气装置,即a开头,装置A中制备的氢气中含有水蒸气,连有干燥装置,根据制备FeCl2的反应方程式,有HCl的生成,HCl污染空气,应用碱石灰吸收,因此a连接f、g,g连接d、c或g连接c、d,d连接b,顺序是 afgde(ed)bc;(3)装置B的作用是吸收反应生成氯化氢气体,防止其污染空气,防止空气中的水蒸气进入装置C与无水氯化亚铁反应;(4)应先熄灭酒精灯,再通一段时间的氢气,让FeCl2冷却,防止被氧气氧化FeCl3;(5)根据反应方程式,求出Fe2+的物质的量为W×3/592mol,200mL的溶液中FeCl2的质量分数为W×3×127×200/(592×20)×100%=1905w/296m×100%,因为Fe2+容易被氧化,因此结果偏低的原因是:在实验过程中会有部分FeCl2被空气中的氧气氧化为FeCl3,使测得的w数值偏小,结果偏低。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】弱酸H2A溶液中存在H2A、HA-和A2- 三种形态的粒子,其物质的量分数 δ( X)=  随溶液pH变化的关系如图所示,下列说法正确的是( )
随溶液pH变化的关系如图所示,下列说法正确的是( )

A. 曲线①代表的粒子是HA-
B. 0.1mol·L -1的NaHA溶液中存在:c(Na+ )+c(A2- )+c(H2A)+c(HA- )>0.2 mol·L-1
C. 若图中的a值为4.2,则H2A的第二步电离平衡常数Ka1为10-4.2
D. 随着PH的升高,  的比值先增大后减小
的比值先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg ![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( ) 
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH﹣)相等
D.当lg ![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25%的酒精密度为0.96 g·cm-3,5%的酒精密度为0.99 g·cm-3。若将上述两溶液等体积混合,所得酒精溶液的质量分数是 ( )
A. 等于15% B. 大于15%
C. 小于15% D. 无法估算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应mX(g)+nY(g)qZ(g),△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列有关说法正确的是( )
A.如果继续通入一定量某气体使体系压强增大,平衡将正向移动
B.此时,X的正反应速率是Y的逆反应速率的 ![]() 倍
倍
C.如果降低温度,且保持物质状态不发生改变,混合气体的平均相对分子质量变小
D.如果增加X的物质的量,平衡正向移动,X的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于胶体和溶液的叙述中正确的是
A. 胶体带电荷,而溶液呈电中性
B. 胶体粒子的直径大小在1-100纳米之间
C. 胶体加入电解质可产生沉淀,而溶液不能
D. 从颜色上无法区别FeCl3溶液和Fe((OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性溶液中只有Na+、CH3COO﹣、H+、OH﹣四种离子.则下列描述正确的是( )
A.该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO﹣)>c(Na+ )>c(OH﹣)>c(H+ )
D.加入适量氨水,c(CH3COO﹣)一定大于c(Na+ )、c(NH ![]() )之和
)之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种离子。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中不正确的是

A.还原剂是含CN-的物质,氧化产物不只有N2
B.氧化剂是ClO-,还原产物是HCO3-
C.参与反应的氧化剂与还原剂的物质的量之比为5:2
D.标准状况下若生成2.24LN2则转移电子为1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com