

| Cu |
| �� |
| Cu |
| �� |
| Ũ���� |
| �� |
| Ũ���� |
| �� |
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�



�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | 0.02mol/LNaHSO3��Һ/mL | 0.02mol/LKIO3��Һ/mL | H2O/mL | ��Ӧ�¶�/�� | ��Һ������ʱ��t/s |
| �� | 15 | 20 | 10 | 15 | t1 |
| �� | a | 30 | 0 | 15 | t2 |
| �� | 15 | b | c | 30 | t3 |
| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ��ʵ������ͽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����Ϊͬϵ�
����Ϊͬϵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� |
| �� |
| �� |
| �� |
| �� |
| 500�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ �� �� �� | �� | �� | �� | �� | �� | |
| �Լ� ���� ��mL�� | 0.20 mol?L-1 ��NH4��2S2O8��Һ | 20.0 | 10.0 | b | 20.0 | 20.0 |
| 0.20 mol?L-1 KI��Һ | 20.0 | 20.0 | 20.0 | 10.0 | 5.0 | |
| 0.010 mol?L-1 Na2S2O3��Һ | a | 8.0 | 8.0 | 8.0 | 8.0 | |
| 0.2% ������Һ | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 0.20 mol?L-1KNO3��Һ | 0 | 0 | 0 | 10.0 | c | |
| 0.20 mol?L-1��NH4��2SO4��Һ | 0 | 10.0 | 15.0 | 0 | 0 | |
| 20��ʱ����Ӧʱ���t��s�� | 32 | 67 | 130 | 66 | 135 | |
| Ϊ��ʹ��Һ������ǿ�Ⱥ���������ֲ��䣬���ٵģ�NH4��2S2O8��Һ��KI��Һ���������ֱ��ã�NH4��2SO4��Һ��KNO3��Һ���㣻��Һ��Ϻ�������� | ||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
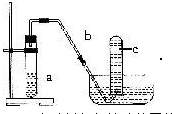
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
c(N
| ||
| c(NH3?H2O)c(H+) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com