

| 催化剂 |
 ,可知A的结构简式为:
,可知A的结构简式为: ,故苯乙烯与(CH3)2C=CH2发生取代反应生成A,
,故苯乙烯与(CH3)2C=CH2发生取代反应生成A, 与HCl反应生成B,结合B的分子式可知,应是发生加成反应,B中核磁共振氢谱图显示分子中有6种不同环境的氢原子,故B为
与HCl反应生成B,结合B的分子式可知,应是发生加成反应,B中核磁共振氢谱图显示分子中有6种不同环境的氢原子,故B为 ,顺推可知C为
,顺推可知C为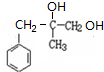 ,D为
,D为 .苯乙烯与水发生加成反应生成E,E可以氧化生成C8H8O2,说明E中羟基连接的C原子上有2个H原子,故E为
.苯乙烯与水发生加成反应生成E,E可以氧化生成C8H8O2,说明E中羟基连接的C原子上有2个H原子,故E为 ,C8H8O2为
,C8H8O2为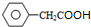 ,
,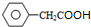 与溴反应生成G,G在氢氧化钠溶液条件下水解、酸化得到H,且D和H是同系物,故
与溴反应生成G,G在氢氧化钠溶液条件下水解、酸化得到H,且D和H是同系物,故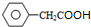 中亚甲基上1个H原子被Br原子取代生成G,G为
中亚甲基上1个H原子被Br原子取代生成G,G为 ,H为
,H为 ,D与H生成W,W结构中含有三个六元环,则W为
,D与H生成W,W结构中含有三个六元环,则W为 ,据此解答.
,据此解答. ,其含有溴原子和羧基两种官能团,故答案为:溴原子、羧基;
,其含有溴原子和羧基两种官能团,故答案为:溴原子、羧基; ,与氯气发生取代反应生成
,与氯气发生取代反应生成 ,
, 与HCl反应生成B,结合B的分子式可知,应是发生加成反应,故答案为:取代反应;加成反应;
与HCl反应生成B,结合B的分子式可知,应是发生加成反应,故答案为:取代反应;加成反应; ,可知A的结构简式为:
,可知A的结构简式为: ,D为
,D为 ,H为
,H为 ,D与H生成W,W结构中含有三个六元环,则W为
,D与H生成W,W结构中含有三个六元环,则W为 ,故答案为:
,故答案为: ;
; ;
; ,H为
,H为 ,有G生成H是卤代烃的水解,卤代烃在氢氧化钠水溶液,加热生成醇,故答案为:氢氧化钠水溶液,加热;
,有G生成H是卤代烃的水解,卤代烃在氢氧化钠水溶液,加热生成醇,故答案为:氢氧化钠水溶液,加热; ,顺推可知C为
,顺推可知C为 ,有B生成C是卤代烃的水解,卤代烃在氢氧化钠水溶液,加热生成醇,化学方程式为:
,有B生成C是卤代烃的水解,卤代烃在氢氧化钠水溶液,加热生成醇,化学方程式为: ;D为
;D为 ,由D通过酯化反应可以生成高分子化合物,其方程式为:
,由D通过酯化反应可以生成高分子化合物,其方程式为: ,
, ;
; ;
;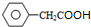 ,其同分异构体能够发生①能发生银镜反应说明含有醛基,②能发生水解反应说明含有酯基,可以是苯酚与甲酸形式的酯,其与苯环上的一个甲基处在邻间对三个位置,有三种同分异构体,还有
,其同分异构体能够发生①能发生银镜反应说明含有醛基,②能发生水解反应说明含有酯基,可以是苯酚与甲酸形式的酯,其与苯环上的一个甲基处在邻间对三个位置,有三种同分异构体,还有 ,共4种同分异构体;其中核磁共振氢谱为5组峰的只有
,共4种同分异构体;其中核磁共振氢谱为5组峰的只有 ,且其峰面积之比为1:2:2:2:1,故答案为:4;
,且其峰面积之比为1:2:2:2:1,故答案为:4; ;1:2:2:2:1.
;1:2:2:2:1.


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇与乙酸都存在碳氧双键 |
| B、油脂水解可得到氨基酸和甘油 |
| C、淀粉和纤维素水解最终产物都是葡萄糖 |
| D、卤代烃加入硝酸酸化的硝酸银溶液可根据生成的卤化银沉淀颜色检验卤原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氟酸的电离方程式及热效应可表示为:HF(aq)?F-(aq)+H-(aq)△H=-10.4kJ?mol-1 |
| B、当V=20时,溶液中:c(OH-)=c(HF)+c(H+) |
| C、当V=20时,溶液中:c(F-)<c(Na+)=0.1mol?L-1 |
| D、当V>0时,溶液中可能存在:c(Na+)>c(F-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、x=2 |
| B、该反应是吸热反应 |
| C、P3>P4,y轴表示B的转化率 |
| D、P3<P4,y轴表示混合气体的密度. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定条件下,对于反应mA(g)+n(B)?cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的△H、△S判断正确的是( )
在一定条件下,对于反应mA(g)+n(B)?cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的△H、△S判断正确的是( )| A、△H<0,△S>0 |
| B、△H>0,△S<0 |
| C、△H>0,△S>0 |
| D、△<0,△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种,若加入锌粒,产生无色无味的气体;若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入的物质的量之间的关系如图所示,下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种,若加入锌粒,产生无色无味的气体;若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入的物质的量之间的关系如图所示,下列说法正确的是( )| A、溶液中一定不含有CO32-,可能含有SO42-和NO3- |
| B、溶液中的阳离子只有H+、Mg2+、Al3+ |
| C、溶液中n(NH4+)=0.2mol |
| D、n(H+):n(Al3+):n(Mg2+)=1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 铵盐质量(g) | 浓硫酸增加的质量(g) |
| 第一次 | 9.05 | 1.7 |
| 第二次 | 18.10 | 1.7 |
| 第三次 | 27.15 | a |
| 第四次 | 36.20 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验方案 | 现象 | 结论 |
| A |  | 向里推活塞时,长颈漏斗中有一段水柱,静止,水柱高度不变 | 该装置的气密性良好 |
| B |  | 脱脂棉燃烧 | Na2O2与水反应生成氢氧化钠和氧气 |
| C |  | 烧杯①的澄清石灰水先变浑浊 | NaHCO3比Na2CO3受热更易分解 |
| D | 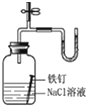 | U形管右端的液面高 | 铁钉发生吸氧腐蚀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com