
 ¶žŃõ»ÆĢ¼ŹĒµŲĒņĪĀŹŅŠ§Ó¦µÄ×ļæż»öŹ×£¬ÄæĒ°ČĖĆĒ“¦Ąķ¶žŃõ»ÆĢ¼µÄ·½·ØÖ®Ņ»ŹĒŹ¹ĘäÓėĒāĘų·“Ó¦ŗĻ³É¼×“¼£®ŅŃÖŖĒāĘų”¢¼×“¼Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
¶žŃõ»ÆĢ¼ŹĒµŲĒņĪĀŹŅŠ§Ó¦µÄ×ļæż»öŹ×£¬ÄæĒ°ČĖĆĒ“¦Ąķ¶žŃõ»ÆĢ¼µÄ·½·ØÖ®Ņ»ŹĒŹ¹ĘäÓėĒāĘų·“Ó¦ŗĻ³É¼×“¼£®ŅŃÖŖĒāĘų”¢¼×“¼Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ| ĪļÖŹ | CH3OH | CH3OCH3 | H2O |
| ÅضČ/£Ømol/L£© | 0.44 | 0.6 | 0.6 |
·ÖĪö £Ø1£©ÓÉ¢Ł2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-283.0 kJ/mol£»
¢Ś2CH3OH£Ø1£©+3O2£Øg£©ØT2CO2£Øg£©+4H2O£Øl£©”÷H=-726.0 kJ/mol£»
øł¾ŻøĒĖ¹¶ØĀÉ£ŗCO2£Øg£©+3H2£Øg£©?CH3OH£Øl£©+H2O£Øl£©”÷H=$\frac{3¢Ł-¢Ś}{2}$£¬½ųŠŠ¼ĘĖćĒó½ā£»
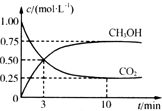
£Ø2£©ĻČøł¾ŻÅØ¶Č±ä»Æ¼ĘĖćĘ½ŗāŹ±ø÷ĪļÖŹµÄÅØ¶Č£¬CH3OHµÄĢå»ż·ÖŹżµČÓŚ¼×“¼µÄĪļÖŹµÄĮæÅضČÓė×ÜĪļÖŹµÄĮæÅضČÖ®±Č£»
£Ø3£©¢Łøł¾Ż·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=$\frac{c£ØC{H}_{3}OC{H}_{3}£©•c£Ø{H}_{2}O£©}{{c}^{2}£ØC{H}_{3}OH£©}$ ¼ĘĖć£»
¢ŚĄūÓĆČż¶ĪŹ½¼ĘĖćĘ½ŗāŹ±ø÷×é·ÖÅØ¶Č£¬øł¾Żv=$\frac{”÷c}{”÷t}$¼ĘĖć·“Ó¦ĖŁĀŹ£»
£Ø4£©¢Ł¼×“¼ŌŚøŗ¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ӧɜ³É¶žŃõ»ÆĢ¼£»
¢ŚŌµē³ŲÖŠŅõĄė×ÓŅĘĻņøŗ¼«£®
½ā“š ½ā£ŗ£Ø1£©ÓÉ¢Ł2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-283.0 kJ/mol£»
¢Ś2CH3OH£Ø1£©+3O2£Øg£©ØT2CO2£Øg£©+4H2O£Øl£©”÷H=-726.0 kJ/mol£»
øł¾ŻøĒĖ¹¶ØĀÉ£ŗCO2£Øg£©+3H2£Øg£©?CH3OH£Øl£©+H2O£Øl£©”÷H=$\frac{3¢Ł-¢Ś}{2}$=$\frac{3”Į£Ø-283.0£©-£Ø-726.0£©}{2}$=-61.5 kJ/mol£¬¹Ź“š°øĪŖ£ŗ-61.5 kJ/mol£»
£Ø2£©æŖŹ¼Ź±c£ØCO2£©=1mol/L”¢c£ØH2£©=3mol/L£¬Ę½ŗāŹ±c£ØCO2£©=0.25mol/L£¬c£ØCH3OH£©=c£ØH2O£©=0.75mol/L£¬Ōņc£ØH2£©=3mol/L-0.75mol/L”Į3=0.75mol/L£¬CH3OHµÄĢå»ż·ÖŹżµČÓŚ¼×“¼µÄĪļÖŹµÄĮæÅضČÓė×ÜĪļÖŹµÄĮæÅضČÖ®±Č£¬ĖłŅŌ¼×“¼µÄĢå»ż·ÖŹż=$\frac{0.75mol}{£Ø0.25+0.75+0.75+0.75£©mol/L}$”Į100%=30%£¬
¹Ź“š°øĪŖ£ŗ30%£»
£Ø3£©¢ŁøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ£ŗK=$\frac{c£ØC{H}_{3}OC{H}_{3}£©•c£Ø{H}_{2}O£©}{{c}^{2}£ØC{H}_{3}OH£©}$£¬½«ĖłøųÅØ¶Č“ųČėĘ½ŗā³£Źż±ķ“ļŹ½£ŗ$\frac{0.6”Į0.6}{0.4{4}^{2}}$=1.86£¼400£¬¹Ź·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¹Ź“š°øĪŖ£ŗ£¾£»
¢Ś2CH3OH£Øg£©ØPCH3OCH3£Øg£©+H2O£Øg£©
ijŹ±æĢÅØ¶Č£Ømol•L-1£©£ŗ0.44 0.6 0.6
×Ŗ»ÆÅØ¶Č£Ømol•L-1£©£ŗ2x x x
Ę½ŗāÅØ¶Č£Ømol•L-1£©£ŗ0.44-2x 0.6+x 0.6+x
K=$\frac{£Ø0.6+x£©^{2}}{£Ø0.44-2x£©^{2}}$=400£¬½āµĆx=0.2mol/L£¬
¹ŹĘ½ŗāŹ±c£ØCH3OH£©=0.44mol/L-0.2mol/L”Į2=0.04mol/L£¬
ĘšŹ¼Ź±ŌŚĆܱÕČŻĘ÷ÖŠ¼ÓČėCH3OH£¬
ŌņĘšŹ¼Ź±¼×“¼µÄÅضČĪŖ0.44moL/L+0.6mol/L”Į2=1.64mol/L£¬Ę½ŗāŹ±c£ØCH3OH£©=0.04mol/L£¬
Ōņ10min×Ŗ»Æ¼×“¼1.64moL/L-0.04moL/L=1.6mol/L£¬
ĖłŅŌ¼×“¼µÄ·“Ó¦ĖŁĀŹĪŖv£ØCH3OH£©=$\frac{”÷c}{”÷t}$=$\frac{1.6mol/L}{10min}$=0.16 mol/£ØL•min£©£¬
¹Ź“š°øĪŖ£ŗ0.16 mol/£ØL•min£©£»
£Ø4£©¢Ł¼×“¼ŌŚøŗ¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬µē¼«·“Ó¦ĪŖ£ŗCH3OH-6e-+3O2-=CO2+2H2O£»¹Ź“š°øĪŖ£ŗCH3OH-6e-+3O2-=CO2+2H2O£»
¢ŚŅĄ¾Żµē¼«·“Ó¦·ÖĪöæÉÖŖŌµē³ŲÖŠŅõĄė×ÓŅĘĻņøŗ¼«£¬ŃõĄė×Ó“ÓÕż¼«Į÷Ļņøŗ¼«ŅĘ¶Æ£»
¹Ź“š°øĪŖ£ŗA£®
µćĘĄ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½ŗĶøĒĖ¹¶ØĀɼĘĖćÓ¦ÓĆ£¬Ōµē³ŲŌĄķ·ÖĪöÅŠ¶Ļ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬×¢Ņā”°Ź¼”¢×Ŗ”¢Ę½”±ŹĒ½ā¾öÓŠ¹Ų»ÆŃ§Ę½ŗāµÄ”°Čż¶ĪĀŪ”±½āĢā·Ø£¬µ±Čż×éĮæŅ»µ©Č·¶Ø£¬æÉŅŌ½ā“šÓŠ¹ŲĘ½ŗāµÄĘ½ŗā³£Źż¼ĘĖć”¢×Ŗ»ÆĀŹ”¢·“Ó¦ĖŁĀŹ”¢Ę½ŗāŹ±³É·ÖµÄĢå»ż·ÖŹżµČµÄ¹Ų¼ü£¬µē¼«·“Ó¦ŹéŠ“·½·Ø£¬×¢Ņāµē½āÖŹŹĒ¹ĢĢ壬ĢāÄæÄѶČÖŠµČ£®


 ·¢É¢Ė¼Ī¬ŠĀæĪĢĆĻµĮŠ“š°ø
·¢É¢Ė¼Ī¬ŠĀæĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 L 0.1 mol•L-1“×Ėį | B£® | 0.1 L 1 mol•L-1H2SO4ČÜŅŗ | ||
| C£® | 0.5 L 0.1mol•L-1ŃĪĖį | D£® | 2 L 0.1mol•L-1 H2SO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪĀ¶Č£Ø”ę£© | 10 | 20 | 30 | ¼ÓČČÖó·ŠŗóĄäČ“µ½50”ę |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ś¢Ū | C£® | ¢Ū¢Ü | D£® | ¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
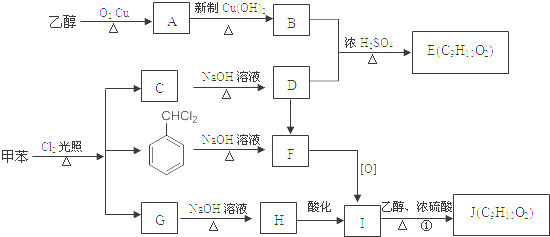

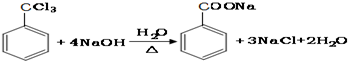 £®
£®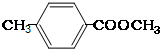 £»¢Ś
£»¢Ś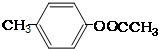 £»¢Ū
£»¢Ū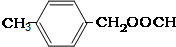 »ņ
»ņ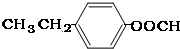 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2øö | B£® | 3øö | C£® | 4øö | D£® | 5øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÕĘųÖŠPM2.5£Ø2.5Ī¢Ć×ŅŌĻĀµÄæÅĮ£Īļ£©µÄ“ęŌŚÄܹ»ŠĪ³É¶”“ļ¶ūŠ§Ó¦ | |
| B£® | ĆŗČ¼ÉÕŹ±¼ÓČėÉŁĮæµÄÉśŹÆ»ŅæÉŅŌ¼õÉŁ·ĻĘųÖŠµÄ¶žŃõ»ÆĮņÅÅ·Å | |
| C£® | ½«ŌģÖ½·ĻĖ®ĶعżøßŃ¹Ė®¾®Ń¹µ½µŲĻĀ£¬½ŚŌ¼Éś²ś³É±¾ | |
| D£® | ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆŗōĪüŌĄķ¶Ō»·¾³ĪŪČ¾½ųŠŠÖĪĄķ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com