
| A. | 100mL12mol/L浓盐酸与足量的MnO2加热充分反应生成氯气分子数为0.3 NA | |
| B. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| C. | 向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移的电子的数目为NA | |
| D. | 5.4g铝粉与足量的氢氧化钠溶液充分反应生成氢气分子数为0.3 NA |
分析 A.稀盐酸与二氧化锰不反应;
B.铁与稀硝酸的反应中,反应产物可能为硝酸亚铁或硝酸铁;
C.碘离子和亚铁离子都能够被氯气氧化且先氧化碘离子再氧化亚铁离子;
D.铝与足量氢氧化钠反应,1个铝原子失去3个电子变成+3价的偏铝酸根离子.
解答 解:A.稀盐酸与二氧化锰不反应,生成氯气分子数小于0.3 NA,故A错误;
B.5.6g铁的物质的量为0.1mol,0.1mol铁与硝酸反应,如果硝酸不足,反应生成0.1mol亚铁离子,失去0.2mol电子,失去的电子为0.2NA,故B错误;
C.FeI2溶液中,碘离子的还原性大于亚铁离子的,通入适量氯气,当有1molFe2+被氧化时,溶液中碘离子已经完全被氧化,由于不知道碘化亚铁的物质的量,无法计算转移的电子数,故C错误;
D.5.4g铝的物质的量为n0.2mol,2Al+2NaOH+2H2O=2NaAlO2+3H2↑由方程式可以看出,反应关系式为2Al~3H2,所以5.4g铝与足量氢氧化钠反应生成氢气分子数为0.3 NA,故D正确.
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项A为易错点,注意稀盐酸与二氧化锰不反应.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
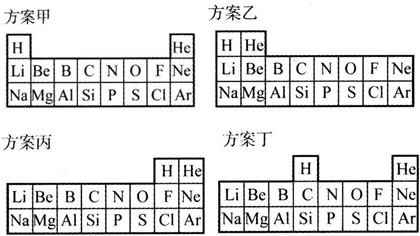
| “合理”的理由 | |
| 方案甲 | |
| 方案乙 | |
| 方案丙 | |
| 方案丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑦⑧⑨ | B. | ②④⑦⑨ | C. | ③④⑦ | D. | ④⑤⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉溶液中加入少许食醋可以增强其漂白效果 | |
| B. | 用二氧化硫漂白米粉是违法行为,因为二氧化硫有毒 | |
| C. | 铝制品在生活中非常普遍,这是因为铝不活泼 | |
| D. | 氢氧化铝可用于治疗胃酸过多,但不宜长期服用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
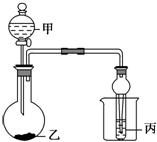 利用图所示装置进行下列实验,能观察到相应现象并得出相应实验结论的是( )
利用图所示装置进行下列实验,能观察到相应现象并得出相应实验结论的是( )| 选项 | 甲 | 乙 | 丙 | 实验现象 | 实验结论 |
| A | 浓盐酸 | 石灰石 | NaAlO2溶液 | 乙中有无色气泡,丙中先出现沉淀后消失 | 氢氧化铝溶于碳酸 |
| B | 浓硫酸 | 蔗糖 | 溴水 | 乙中蔗糖变黑色、丙中溴水褪色 | 浓硫酸具有脱水性、氧化性 |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | 乙中有无色气泡,丙中出现白色沉淀 | SO2与可溶性钡盐均可生成白色沉淀 |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 乙中有无色气泡,丙中出现白色沉淀 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2n(C)+n(N)+2 | B. | 2n(C)+2n(N)+n(O) | C. | 3n(C)+2n(O)+2 | D. | 2n(C)+2n(N)+2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol Na2CO3和1.6mol NaOH | B. | 1mol Na2CO3与0.6mol NaHCO3 | ||
| C. | 0.8mol Na2CO3和1mol NaOH | D. | 1mol Na2CO3和0.6mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
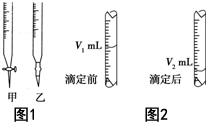 现用物质的量浓度为a mol•L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
现用物质的量浓度为a mol•L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com