
| a | | | |||||||||||||||
| | | | | f | y | h | i | | |||||||||
| | b | | e | | | | j | | |||||||||
| c | | | | | | | d | [ | d | | g | | l | | | | |
| | | | [ | | | | | | | | | | | | | | |
科目:高中化学 来源:不详 题型:单选题
| A.钚是f 区元素 | B..核外电子数238 |
| C.核内中子数 144 | D.钚是锕系元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.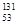 I和 I和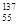 Cs的核内中子数分别为53和55 Cs的核内中子数分别为53和55 |
B.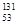 I2不能升华 I2不能升华 |
C.标准状况下,22.4L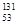 I2中约含有156×6.02×1023个中子 I2中约含有156×6.02×1023个中子 |
D.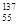 Cs原子最外层电子数为1 Cs原子最外层电子数为1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一 |
| B.元素周期表中,总共有18个纵行,16个族,过渡元素都为副族元素 |
| C.在周期表中,第ⅡA族元素都为金属元素 |
| D.X3+的核外电子数目为10,则X在第三周期第ⅢA族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,分子中C原子的杂化轨道方式是_____________;按原子轨道重叠方式判断COCl分子中的化学键类型为___________________。
,分子中C原子的杂化轨道方式是_____________;按原子轨道重叠方式判断COCl分子中的化学键类型为___________________。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.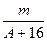 (A-n+8)mol (A-n+8)mol | B.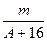 (A-n+10)mol (A-n+10)mol |
| C.(A-n+2)mol | D.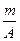 (A-n+6)mol (A-n+6)mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com