
| A. | c=$\frac{b}{11.2V}$ | B. | p=m+$\frac{{V}_{c}}{125}$ | C. | n=m+17Vc | D. | $\frac{17}{9}$m<p<$\frac{5}{3}$m |
分析 反应化学方程式为:Mg+H2SO4=MgSO4+H2↑;2Al+3H2SO4=Al2(SO4)3+3H2↑;MgSO4+2KOH=Mg(OH)2↓+K2SO4;Al2(SO4)3+6KOH=2Al(OH)3↓+3K2SO4;Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O;2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;
A.根据n=$\frac{V}{Vm}$计算氢气的物质的量,根据电荷守恒,氢氧化镁、氢氧化铝沉淀中含有n(OH-)等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,据此计算氢氧根离子的物质的量,再根据c=$\frac{n}{V}$计算氢氧化钾的物质的量浓度;
B.由Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O,2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O可知,沉淀灼烧生成氧化镁与氧化铝,二者质量等于金属质量与氧原子的质量之和,由方程式可知氧原子的物质的量等于氢氧根离子物质的量的一半,据此计算;
C.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,根据n=cVM计算氢氧根离子的质量;
D.按照极值方法计算,若mg全是镁,计算生成得到的氧化镁质量,若mg全是铝,计算得到的氧化铝的质量,实际固体的质量介于二者之间.
解答 解:A.根据电荷守恒,氢氧化镁、氢氧化铝沉淀中含有n(OH-),等于金属提供的电子的物质的量,等于生成氢气的获得的电子的物质的量,故生成的氢气的物质的量等于参加反应的碱的物质的量的一半,故$\frac{bL}{22.4L/mol}$×2=cmol/L×V×10-3L,整理得c=$\frac{1000b}{11.2V}$,故A错误;
B.选项中p为生成的氧化物的质量,由Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O,2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O可知,氧化物的质量等于金属质量与氧原子的质量之和,由方程式可知氧原子的物质的量等于氢氧根离子物质的量的一半,故p=m+c×V×10-3×$\frac{1}{2}$×16=m+$\frac{CV}{125}$,故B正确;
C.沉淀为氢氧化镁、氢氧化铝,其质量等于金属的质量与含有的氢氧根离子的质量之和,故n=m+c×V×10-3×17=m+$\frac{17VC}{1000}$,故C错误;
D.得到的氧化物为氧化镁,根据元素守恒,则质量为P=$\frac{m}{24}$×40=$\frac{5m}{3}$,若mg全是铝,得到的氧化物为氧化铝,根据元素守恒,则质量为p=$\frac{m}{27}$×$\frac{1}{2}$×102=$\frac{17m}{9}$,质量介于二者之间,即:$\frac{5}{3}$m<p<$\frac{17}{9}$m,故D错误;
故选:B.
点评 本题综合考查镁铝元素单质及化合物的性质、混合物的有关计算,注意利用方程式与电子转移守恒寻找关系解答,题目计算量较大,且为无数据计算,难度较大.


科目:高中化学 来源: 题型:实验题
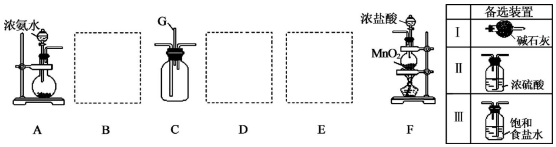
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应 KClO3+6HCl═KCl+3Cl2↑+3H2O 中,Cl2既是氧化产物又是还原产物,当得到标准状况下的 67.2 L Cl2 时,反应中转移的电子数为 5NA | |
| B. | 标准状况下,22.4 L 甲苯中含有的 C-H 键数目为 8NA | |
| C. | 50 g 46%的乙醇水溶液中,含氢原子总数目为 3NA | |
| D. | t℃时,MgCO3的 Ksp=4×10-6,则该温度下饱和 MgCO3溶液中含有的 Mg2+数目为 2×10-3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| B. | Al(OH)3可作阻燃剂,因此可以用于灭火 | |
| C. | SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱 | |
| D. | 焰火的五彩缤纷是某些金属元素的性质的展现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40g NaOH溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成1L溶液 | |
| C. | 从100mL 10mol•L-1的浓盐酸中取出10mL | |
| D. | 20g NaOH溶解在水中配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
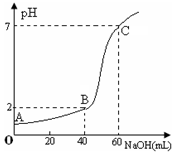 常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示.下列叙述不正确的是( )
常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示.下列叙述不正确的是( )| A. | 所用盐酸的浓度是0.09mol•L─1,NaOH溶液浓度为0.03mol•L─1 | |
| B. | 在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+) | |
| C. | A、B、C三点水的电离程度大小依次为:C>B>A | |
| D. | 滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
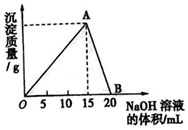 向20ml某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:
向20ml某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{n(m-x)}{m}$ | B. | $\frac{n(m-x+2)}{m}$ | C. | $\frac{m-x+2}{m-x}$ | D. | $\frac{n(m-x-2)}{m}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com