
分析 维生素C是一种重要的维生素,能防治坏血病,又称为抗坏血酸;维生素可分为分为脂溶性维生素和水溶性维生素两类,维生素B、维生素C属于水溶性维生素.
解答 解:维生素C的化学式为C6H8O6,人体缺乏维生素C易得坏血症,所以维生素C又称抗坏血酸;维生素是生物的生长和代谢所必需的微量有机物,维生素可分为分为脂溶性维生素和水溶性维生素两类,脂溶性维生素包括维生素A、维生素D、维生素E、维生素K等,水溶性维生素溶于水而不溶于脂肪,在体内不能储存.有B族维生素和维生素C,
故答案为:抗坏血酸;维生素B、维生素C.
点评 本题考查人体必需的维生素的主要来源及其摄入途径,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | H3PO4的摩尔质量为98 | |
| B. | 阿伏伽德罗常数即为0.012kg12C所含的碳原子数 | |
| C. | 任何气体的摩尔体积均约为22.4L.mol-1 | |
| D. | 一个标准大气压下4℃时,9mL水中所含电子数约为3.01×1024. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L乙醇中含有的碳氢键数为2.5NA | |
| B. | 常温常压下,28gC2H4、CO的混合气体中含有碳原子的数目为1.5NA | |
| C. | 常温下,20LpH=12的Na2CO3溶液中含有的OH-离子数为0.2NA | |
| D. | 标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
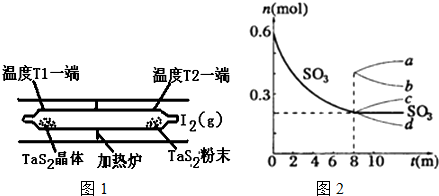
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mo1•L-1MgCl2溶液中含C1一数为0.2 NA | |
| B. | 标准状况下,22.4L的CCl4中含CCl4分子数为NA | |
| C. | 0.1molNa2O2与足量的CO2完全反应转移电子数目为0.1NA | |
| D. | 10mL5mol•L-1(NH4)2CO3溶液中含有N原子数目小于0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加压有利于化学平衡向正反应方向移动 | |
| B. | 该反应的化学平衡常数表达式为:K=$\frac{{c}^{2}{N}_{2}{H}_{4}×{c}^{2}N{O}_{2}}{{c}^{3}{N}_{2}×{c}^{4}{H}_{2}O}$ | |
| C. | 升高温度可缩短反应达平衡的时间但不能提高平衡转化率 | |
| D. | 使用催化剂可缩短反应达平衡的时间但不能提高平衡转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的N2与O2中的所含分子数均为NA | |
| B. | 标准状况下,5.6L CCl4含有的分子数为0.25NA | |
| C. | 常温常压下,22gCO2含有的原子数为1.5NA | |
| D. | 1mol/L NaOH溶液中含有的Na+的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com