
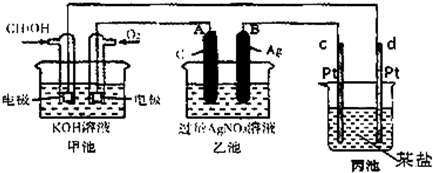
分析 燃料电池中,通入燃料的电极为负极,电极反应为CH3OH+8OH--6 e-=CO32-+6H2O,通入氧化剂的电极为正极,正极反应为O2+4e-+2H2O=4OH-,A是阳极、B是阴极,阳极、阴极电极反应分别为4OH--4e-=O2↑+2H2O、Ag++e-=Ag,c是阳极、d为阴极,以此解答该题.
解答 解:(1)甲为燃料电池,为原电池,化学能转化为电能,故答案为:原电池;
(2)通入甲醇的电极为负极,电极反应为CH3OH+8OH--6 e-=CO32-+6H2O,故答案为:CH3OH+8OH--6 e-=CO32-+6H2O;
(3)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加10.8g时,n(Ag)=0.1mol,
则转移电子为0.1mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.1mol电子时消耗的氧气为0.025mol,则氧气的体积为0.025mol×22.4L/mol=0.56L=560mL;
丙池是电解池,阴极上金属离子放电析出金属单质,则金属元素在氢元素之后,则溶液是硫酸铜溶液,也可能是硝酸银,故选BD.
故答案为:560; BD.
点评 本题考查了原电池原理和电解池原理,为高频考点,明确原电池和电解池电极上发生反应的类型即可分析解答本题,难度不大,注意电极反应式的书写.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示的装置为铁的吸氧腐蚀实验.一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,可观察到现象为铁钉附近的溶液有蓝色沉淀,该反应的离子方程式为Fe2++[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓; 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为O2+4e-+2H2O=4OH.
如图所示的装置为铁的吸氧腐蚀实验.一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,可观察到现象为铁钉附近的溶液有蓝色沉淀,该反应的离子方程式为Fe2++[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓; 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为O2+4e-+2H2O=4OH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
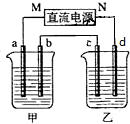 如图所示装置中,甲、乙两个烧杯分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙两个烧杯分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,电极均为石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
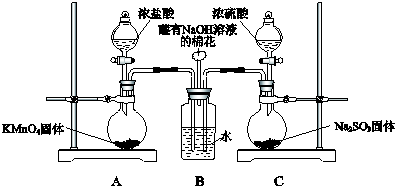
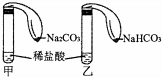 为对比Na2CO3与NaHCO3的性质,实验小组的同学们在甲、乙两支试管中分别加入足量稀盐酸,将两个分别装有Na2CO3或NaHCO3粉末的小气球分别套在两支试管口.将气球内的Na2CO3或NaHCO3倒入试管中(如图).
为对比Na2CO3与NaHCO3的性质,实验小组的同学们在甲、乙两支试管中分别加入足量稀盐酸,将两个分别装有Na2CO3或NaHCO3粉末的小气球分别套在两支试管口.将气球内的Na2CO3或NaHCO3倒入试管中(如图).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为16、中子数为17的硫原子:$\stackrel{17}{16}S$ | |
| B. | 硫离子(S2-)的结构示意图: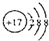 | |
| C. | 二硫化碳分子的结构式:S=C=S | |
| D. | 硫化氢分子的电子式: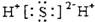 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com