
| A£® | Ļą¶ŌŌ×ÓÖŹĮæ£ŗAr£¾K | B£® | ¼īŠŌ£ŗNaOH£¾Mg£ØOH£©2 | ||
| C£® | ĖįŠŌ£ŗHNO3£¾H3PO4 | D£® | ŌŖĖŲ·Ē½šŹōŠŌ£ŗCl£¾S |
·ÖĪö A£®Ļą¶ŌŌ×ÓÖŹĮæµÄ“óŠ”ÓėŌ×ÓŠņŹżÓŠ¹Ų£»
B£®ŌŖĖŲµÄ½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌŌ½Ē棻
C£®ŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌŌ½Ē棻
D£®Ķ¬ÖÜĘŚŌŖĖŲ“Ó×óµ½ÓŅ£¬ŌŖĖŲµÄ½šŹōŠŌÖš½„¼õČõ£®
½ā“š ½ā£ŗA£®Ļą¶ŌŌ×ÓÖŹĮæµÄ“óŠ”ÓėŌ×ÓŠņŹżÓŠ¹Ų£¬ĖęŌ×ÓŠņŹżµÄŌö“ó¶ųŌö“󣬓ęŌŚÖÜĘŚŠŌµÄ±ä»Æ£¬²»ÄÜÓĆŌŖĖŲÖÜĘŚĀɽāŹĶ£¬¹ŹAŃ”£»
B£®Na”¢MgĪ»ÓŚÖÜĘŚ±ķĻąĶ¬ÖÜĘŚ£¬½šŹōŠŌNa£¾Mg£¬ŌŖĖŲµÄ½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌŌ½Ē棬ÄÜÓĆŌŖĖŲÖÜĘŚĀɽāŹĶ£¬¹ŹB²»Ń”£»
C£®·Ē½šŹōŠŌN£¾P£¬ŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦µÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌŌ½Ē棬ÄÜÓĆŌŖĖŲÖÜĘŚĀɽāŹĶ£¬¹ŹC²»Ń”£»
D£®Ķ¬ÖÜĘŚŌŖĖŲ“Ó×óµ½ÓŅ£¬ŌŖĖŲµÄ·Ē½šŹōŠŌÖš½„ŌöĒ棬ÄÜÓĆŌŖĖŲÖÜĘŚĀɽāŹĶ£¬¹ŹD²»Ń”£®
¹ŹŃ”£ŗA£®
µćĘĄ ±¾Ģā²ąÖŲÓŚŌŖĖŲÖÜĘŚĀɵĥķ½āÓėÓ¦ÓƵÄ漲飬עŅā°ŃĪÕŌŖĖŲÖÜĘŚĀɵĵŻ±ä¹ęĀÉŅŌ¼°Ļą¹ŲÖŖŹ¶µÄ»żĄŪ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
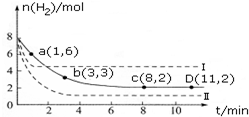 ¹¤ŅµÉĻŃŠ¾æĄūÓĆCO2Ą“Éś²ś¼×“¼Č¼ĮĻµÄ·½·Ø£¬øĆ·½·ØµÄČČ»Æѧ·½³ĢŹ½ŹĒ£ŗ
¹¤ŅµÉĻŃŠ¾æĄūÓĆCO2Ą“Éś²ś¼×“¼Č¼ĮĻµÄ·½·Ø£¬øĆ·½·ØµÄČČ»Æѧ·½³ĢŹ½ŹĒ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
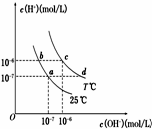 ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬Ė®ČÜŅŗÖŠc£ØH+£©Óėc£ØOH-£©ÓŠČēĶ¼ĖłŹ¾¹ŲĻµ£®ĻĀĮŠĢõ¼ž¹ŲÓŚĄė×Ó¹²“ęĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬Ė®ČÜŅŗÖŠc£ØH+£©Óėc£ØOH-£©ÓŠČēĶ¼ĖłŹ¾¹ŲĻµ£®ĻĀĮŠĢõ¼ž¹ŲÓŚĄė×Ó¹²“ęĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | aµć¶ŌÓ¦µÄČÜŅŗÖŠ“óĮæ“ęŌŚ£ŗFe3+”¢Ba2+”¢K+”¢NO3- | |
| B£® | bµć¶ŌÓ¦µÄČÜŅŗÖŠ“óĮæ“ęŌŚ£ŗNa+”¢K+”¢NH4+”¢Cl- | |
| C£® | dµć¶ŌÓ¦µÄČÜŅŗÖŠ“óĮæ“ęŌŚ£ŗNa+”¢Ba2+”¢Cl-”¢Al3+ | |
| D£® | cµć¶ŌÓ¦µÄČÜŅŗÖŠ“óĮæ“ęŌŚ£ŗCO32-”¢Na+”¢Cu2+”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol¼×»łÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ10NA | |
| B£® | 1molŅŅ“¼ÖŠŗ¬ÓŠC-H¼üµÄŹżÄæĪŖ6NA | |
| C£® | 300mL2mol/LŅŅ“¼Ė®ČÜŅŗÖŠĖłŗ¬HŌ×ÓŹżĪŖ3.6NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬7.0gŅŅĻ©Óė±ūĻ©µÄ»ģŗĻĪļÖŠŗ¬ÓŠĒāŌ×ӵďżÄæĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ż | B£® | ¢Ł¢Ü¢Ž¢ß | C£® | ¢Ś¢Ü¢Ž¢ß | D£® | ¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē×ÓÓÉŠæʬĮ÷³ö | |
| B£® | Šæ±ČĶ»īĘĆ£¬ĖłŅŌŠæ×÷Õż¼« | |
| C£® | ČÜŅŗÖŠc£ØH+£©¼õŠ” | |
| D£® | µ±ÓŠ6.5gŠæČܽāŹ±µēĀ·ÖŠ×ŖŅʵĵē×ÓŹżŹĒ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬CĪŖHOOC-COOH£®AµÄŗģĶā¹āĘ×Ķ¼ŗĶŗĖ“Ź²ÕńĒāĘ×Ķ¼ČēĶ¼1£ŗ
£¬CĪŖHOOC-COOH£®AµÄŗģĶā¹āĘ×Ķ¼ŗĶŗĖ“Ź²ÕńĒāĘ×Ķ¼ČēĶ¼1£ŗ



 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com