
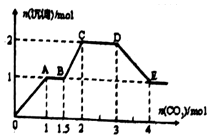
 现有易溶强电解质的混合溶液10L,共中可能含K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与遇入CO2的量之问的关系如图所示,下列说法正确的是( )
现有易溶强电解质的混合溶液10L,共中可能含K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与遇入CO2的量之问的关系如图所示,下列说法正确的是( )| A. | 该溶液中能确定存在的离子是Ba2+、Na+、Cl-、NH4+ | |
| B. | 肯定不存在的离子是Cl-、OH- | |
| C. | 若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为:0.2mol/L | |
| D. | OA段反应的离子方程式::2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
分析 通入二氧化碳,在OA段产生沉淀,说明一定含Ba2+,根据离子共存条件,一定不含SO42-,因二者反应会生成硫酸钡沉淀;在BC段产生沉淀,说明含AlO2-,AlO2-存在碱性环境,故一定含OH-,不含NH4+,因NH4+与OH-反应放氨气,根据OA段,通入1mol二氧化碳生成1mol沉淀,所以 Ba2+为1mol,反应方程式为:Ba(OH)2+CO2=BaCO3↓+H2O,AB段沉淀不变,说明二氧化碳和OH-反应,结合OA段可知含 OH-共3mol,根据BC段可知发生反应:2AlO2-+CO2+3H2O═2A l(OH)3↓+CO32-,故消耗二氧化碳0.5mol,即AlO2-的物质的量为1mol,CD段发生反应:CO32-+CO2+H2O═2HCO3-,DE段发生反应:BaCO3+CO2+H2O═Ba2++2HCO3-,根据电荷守恒,所含阳离子所带正电荷为Ba2+所带:2mol,阴离子所带负电荷为AlO2-、OH-所带:3mol+1mol=4mol,故一定还含阳离子,根据电荷守恒,计算出所含阳离子物质的量,进而计算出浓度.
解答 解:A、根据以上分析可知,一定含Ba2+、AlO2-、OH-,一定不含:NH4+、SO42-,不能确定离子中至少还存在一种阳离子存在,所给阳离子中还有K+、Na+没确定,故A错误;
B、根据以上分析可知,一定含Ba2+、AlO2-、OH-,一定不含:NH4+、SO42-,故B错误;
C、不能确定离子中至少还存在一种阳离子存在,所给阳离子中还有K+、Na+没确定,当不含氯离子,则阳离子浓度最小,根据电荷守恒,所含离子的物质的量设为n,则有:n+2mol=4mol,n=2,浓度为:$\frac{2mol/L}{10L}$=0.2mol/L,故C正确;
D、根据以上分析可知,OA段反应的离子方程式:Ba2++2OH-+CO2=BaCO3↓+H2O,BC段发生反应:2AlO2-+CO2+3H2O═2A l(OH)3↓+CO32-,故D错误;
故选:C.
点评 本题考查了离子的推断,难度较大,关键是搞清反应原理结合离子共存和电荷守恒解答.


科目:高中化学 来源: 题型:选择题
| A. | 用加酶洗衣粉洗衣服时水的温度越高越好 | |
| B. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关 | |
| C. | 小苏打是制作馒头的膨松剂,苏打是治疗胃酸过多的抗酸剂 | |
| D. | 乙醇、过氧化氢、次氯酸钠等消毒液的消毒原理都是利用其强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇中的水(新制CaO) | B. | 乙烷中乙烯(溴水) | ||
| C. | 苯中的甲苯(溴水) | D. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com