
 元素的质量分数为26.7%,其余为N、S。
元素的质量分数为26.7%,其余为N、S。 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源:不详 题型:填空题
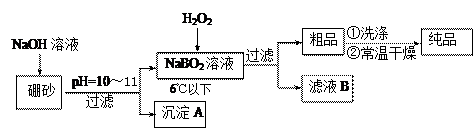

 体中将混有NaBO2 ,则产品中钠的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
体中将混有NaBO2 ,则产品中钠的质量分数 ▲ (填 “升高”、“降低”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
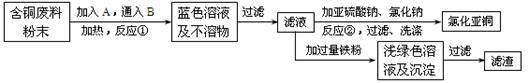
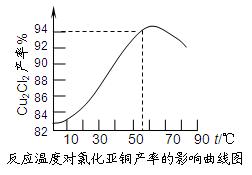
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
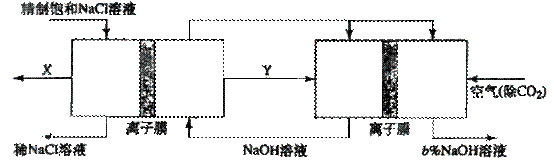
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
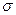 键处1个
键处1个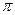 键
键 >CO2
>CO2 5SH>C2H5OH
5SH>C2H5OH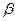 -ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
-ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。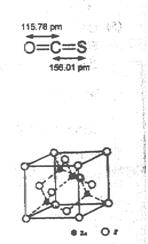
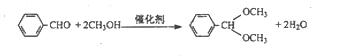
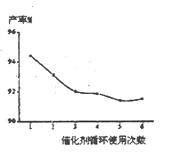
 (3)不同铌酸用量对产率和转化率影响,如下表:
(3)不同铌酸用量对产率和转化率影响,如下表:| 铌酸用量/mol | 0.01 | 0.02 | 0.03 | 0.05 | 0.1 | 0.15 | 0.2 | 0.6 |
| 产率% | 87.3 | 88.2 | 90.3 | 94.2 | 92.9 | 93.1 | 91.8 | 92.3 |
| 转化率% | 89.7 | 92.1 | 93.9 | 98.9 | 94.9 | 95.7 | 93.9 | 94.3 |
| 序号 | 醛 | 醇 | 转化率% | 产率% |
| 1 | 邻羟基苯甲醛 | 甲醇 | 94.3 | 89.6 |
| 2 | 邻羟基苯甲醛 | 甲醇 | 93.6 | 88.7 |
| 3 | 邻氯苯甲醛 | 甲醇 | 93.1 | 87.3 |
| 4 | 间硝基苯甲醛 | 甲醇 | 54.2 | 34.1 |
| 5 | 邻硝基苯甲醛 | 甲醇 | 89.9 | 79.5 |
| 6 | 对硝基苯甲醛 | 甲醇 | 65.7 | 41.9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 后产物可以用于漂白消毒。根据以上信息完成下列化学方程式:
后产物可以用于漂白消毒。根据以上信息完成下列化学方程式:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g) △H<0,在上述条件下,SO2的转化率约为90%。但是部分发达国家采用高压条件获得SO3 ,采取加压措施的目的
2SO3(g) △H<0,在上述条件下,SO2的转化率约为90%。但是部分发达国家采用高压条件获得SO3 ,采取加压措施的目的| A.发达国家电能过量,以此消耗大量能源 |
| B.高压将使平衡向正反应方向移动,有利于进一步提高SO2的转化率 |
| C.加压可使SO2全部转化为SO3 ,消除SO2对空气的污染 |
| D.高压有利于加快反应速率,提高生产效率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业生产硫酸时,使用热交换器可以充分利用反应中所放出的热量 |
| B.工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的 |
| C.工业上用离子交换膜法电解饱和食盐水制烧碱 |
| D.工业上采用电解熔融氯化铝的方法制取金属铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com