
下列关于氯水的说法正确的是( )
|
| A. | 向氯水中通入少量二氧化硫,氯水的漂白性增强 |
|
| B. | 氯水中加入NaCl固体,对溶液的pH无影响 |
|
| C. | 常温下,pH=2的氯水中:c(Cl﹣)+c(ClO﹣)+c(OH﹣)=0.01mol/L |
|
| D. | 向氯水中滴加少量NaHCO3溶液的离子反应方程式为:Cl2+2HCO3﹣═2CO2↑+Cl﹣+ClO﹣+H2O |
| 氯气的化学性质. | |
| 专题: | 卤族元素. |
| 分析: | A.向氯水中通入少量二氧化硫,发生氧化还原反应生成硫酸和盐酸; B.氯水中加入NaCl固体,氯离子浓度增大,Cl2+H2O⇌HCl+HClO逆向移动; C.pH=2的氯水,c(H+)=0.01mol/L,结合电荷守恒分析; D.氯水中滴加少量NaHCO3溶液,盐酸与其反应生成NaCl、水、二氧化碳. |
| 解答: | 解:A.向氯水中通入少量二氧化硫,发生氧化还原反应生成硫酸和盐酸,氯水的漂白性减弱,故A错误; B.氯水中加入NaCl固体,氯离子浓度增大,Cl2+H2O⇌HCl+HClO逆向移动,氢离子浓度减小,pH增大,故B错误; C.pH=2的氯水,c(H+)=0.01mol/L,由电荷守恒可知,c(H+)=c(Cl﹣)+c(ClO﹣)+c(OH﹣)=0.01mol/L,故C正确; D.氯水中滴加少量NaHCO3溶液,盐酸与其反应生成NaCl、水、二氧化碳,发生的离子反应为Cl2+H2O⇌H++Cl﹣+HClO、H++HCO3﹣═CO2↑+H2O,故D错误; 故选C. |
| 点评: | 本题考查氯气的化学性质,为高频考点,综合考查元素化合物性质,涉及氧化还原反应、化学平衡、离子反应等,综合性较强,题目难度不大,选项D为易错点. |


科目:高中化学 来源: 题型:
现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)
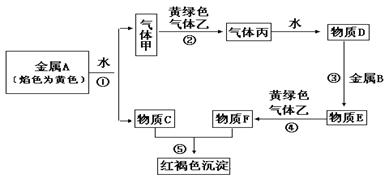
请回答下列问题:
(1)A的化学式为 ,丙的化学式为 ;
(2)写出下列反应的离子方程式:
① ;
④ ;
⑤ 。
(3)写出C溶液与Al反应的化学方程式: 。
(4)将Na2O2投入到E溶液中,可以观察到的现象是: 。
(5)为鉴定B单质,将试样溶于稀盐酸,取上层清液后需再加入的试剂(填写字母代号)是 。
a. 碘水 b. 氯水 c. NaOH溶液 d. KSCN溶液 e. Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A.HF稳定性比HCl强 B.Mg失电子能力比Ca弱
C.NaCl与NH4Cl含有的化学键类型相同 D.等物质的量的C2H6和H2O2含电子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年10月24日双鸭山市区发生严重的雾霾天气,对人们的健康造成严重威胁,环境问题离我们也并不遥远了,则下列有关环境问题说法正确的是( )
A. PH<7的雨水称为酸雨
B. 二氧化硫的大量排放是造成光化学烟雾的主要原因
C. PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生相关
D. SO2、CO2、NO2均属于大气污染物
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、NH4+、Cl﹣、SO42﹣、NO3﹣中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
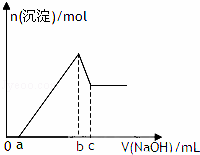
|
| A. | 一定没有Cu2+、NO3﹣、Cl﹣ | B. | 可能有K+、NH4+、NO3﹣、SO42﹣ |
|
| C. | 不能确定是否含有K+、NO3﹣ | D. | 一定有Mg2+、Al3+、Cl﹣、SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应N2O4⇌2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点).下列说法正确的是( )
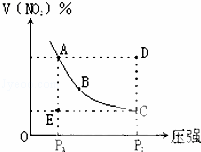
|
| A. | A、C两点的正反应速率的关系A>C |
|
| B. | A、B、C、D、E各状态,V正<V逆的是状态E |
|
| C. | 维持P1不变,E→A所需时间为x,维持P2不变,D→C所需时间为y,则x<y |
|
| D. | 使E状态从水平方向到达C状态,从理论上来讲,可选用的条件是从P1突然加压至P2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸(H2C2O4)是二元中强酸,酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.
Ⅰ、某探究小组利用该反应,用浓度为0.1000mol•L﹣1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的离子方程式为 2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O .
(2)滴定过程中操作滴定管的图示正确的是 A .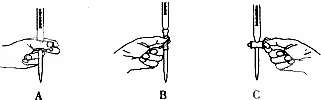
(3)本滴定达到终点的标志是: 当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点
(4)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度 偏高 ,
(填“偏高”、“偏低”、或“不变”).
Ⅱ、草酸氢钠溶液显酸性,常温下,向10mL 0.01mol/LNaHC2O4溶液中滴加0.01mol/LNaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是: BD
A、V(NaOH)=0时,c(H+)=1×10﹣2 mol/L
B、V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42﹣)+c(HC2O4﹣)
C、V(NaOH)=10mL时,c(H+)=1×10﹣7 mol/L
D、V(NaOH)>10mL时,c(Na+)>c(C2O42﹣)>c(HC2O4﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银):n(硝酸亚汞)=2:1,则下列叙述正确的是( )
|
| A. | 电解后溶液的pH都增大 |
|
| B. | 在两个阳极上得到的产物的物质的量不相等 |
|
| C. | 硝酸亚汞的分子式为Hg2(NO3)2 |
|
| D. | 在两个阴极上得到的银和汞的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质属于同分异构体的是( )
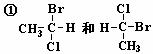
②乙醚和乙醇③乙酸和甲酸甲酯④淀粉和纤维素
⑤苯甲醇和甲基苯酚
⑥葡萄糖和果糖⑦丙烯酸和油酸⑧丙醛和丙烯醇
A.①②④⑦ B.②④⑥⑧ C.③⑤⑥⑧ D.①④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com