
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
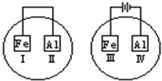
| A、II和Ⅳ | B、Ⅱ和Ⅲ |
| C、Ⅰ和Ⅲ | D、Ⅰ和Ⅳ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X2 |
| B、Y2X2 |
| C、XY2 |
| D、X2Y4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-的水解方程式可表示为:HCO3-+H2O═H3O++CO32- |
| B、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| C、向NaAlO2溶液中通入过量的CO2制Al(OH)3↓2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| D、将16g铁粉投入100mL 4.0mol/L的HNO3溶液中,(还原产物只有NO)3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、仅③ |
| C、仅⑤ | D、②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①② | C、③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若甲、乙两容器均为恒容容器,则x必等于2 |
| B、若甲、乙两容器均为恒压容器,则x必等于3 |
| C、若甲为恒容容器、乙为恒压容器,且 x=3,则 n1必大于n2 |
| D、若甲为恒压容器、乙为恒容容器,且 x≠3,则 n1必大于n2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com